ДОЗИМЕТРИЧЕСКИЕ ПРИБОРЫ
Приборы, которые служат для изучения и контроля ионизирующих излучений, называются дозиметрическими.
Дозиметрические приборы условно можно разделить на пять основных видов: индикаторы, спектроскопы, рентгенометры, радиометры, дозиметры.
Индикаторы – приборы для обнаружения и ориентировочной оценки радиационного поля.
Спектроскопы – служат для определения вида излучения и его энергетического спектра.
Рентгенометры – применяются для измерения экспозиционной дозы и мощности рентгеновского и γ-излучения.
Радиометры – предназначены для измерения активности нуклида или плотности потока частиц.
Дозиметры – используются для измерения дозы или мощности дозы ионизирующего излучения.
Основной узел любого дозиметра - это детектор ионизирующего излучения – устройство, обеспечивающее преобразование энергии ионизирующего излучения в другой вид энергии удобной для регистрации: электрический ток, заряд или электрический импульс. С некоторой условностью детекторы можно разделить на три группы: следовые (или трековые), счётчики, интегральные.
|
|
|
Следовые названы так потому, что позволяют наблюдать трек (траекторию движения) частиц радиоактивного излучения. К ним относятся: камера Вильсона, пузырьковая камера, искровая камера, фотопластинки и фотоэмульсии.
Счётчики регистрируют каждый случай попадания в объём детектора отдельных квантов ионизирующего излучения:
а) сцинтилляционные счётчики – в основе работы лежит явление флуоресценциии;
б) полупроводниковые – реагируют на взаимодействие с частицами радиоактивного излучения изменением электропроводности р-п перехода;
в) черенковские – счётчики, действие которых основано на явлении Вавилова-Черенкова;
г) газоразрядные счётчики – детекторы, в которых используется явление возникновения разряда в газах под воздействием отдельного кванта ионизирующего излучения.
Интегральные детекторы – позволяют зафиксировать суммарную энергию ионизирующего излучения за какое-то время: ионизационная камера, счётчик Гейгера-Мюллера, фотодетектор.
Липидный компонент мембран определяет механические, оптические, электрические (R, C) и осмотические (непроницаемость для ионов и проницаемость для воды) свойства.
С точки зрения электродинамики мембрана представляет собой диэлектрик с относительной диэлектрической проницаемостью от 2 до 6. Селективная проницаемость мембран и различия в концентрации для ионов разных знаков приводит к образованию двойного электрического слоя. Экспериментально показано, что между внутренней и наружной сторонами мембраны существует разность потенциалов в 50-80 мВ (в некоторых случаях более 200 мВ). Учитывая толщину мембраны (7-8 нм), это даёт для напряженности электрического поля в мембране ~ 104 ÷ 105 В·см–1 (пробой воздуха происходит при напряжённости 3∙104 В·см–1).
|
|
|
Поверхность мембраны представляют собой границу раздела: вода-белок. Силы поверхностного натяжения, действующие на этой границе, стремятся сократить площади белковых монослоёв на внутренней и наружной поверхностях мембраны. Это приводит к сжатию липидного бислоя. Измерения коэффициента поверхностного натяжения дали значения 0,1 ÷ 1 мН/м, что хорошо согласуется с данными по белкам.
Вязкость липидного слоя мембран на два порядка выше вязкости воды и равна 30÷100 мПа·с (сравнима с вязкостью подсолнечного масла). Многие болезни связаны с отклонением микровязкости липидной фазы от нормы. Например, канцерогенез связан со снижением ее, а при старении организма вязкость возрастает.
Изменение состояния липидной молекулы, связанное с изменением температуры или химической модификацией жирнокислотного "хвоста", или же с изменением заряда головки, сопровождается изменением площади, которая приходится в мембране на одну молекулу. К такому же результату приводит воздействие на мембраны лекарственных препаратов, например, анестетиков.
Липиды биологических мембран при обычных физиологических условиях (температура, давление, химический состав окружающей среды и т.д.) находятся преимущественно в жидкокристаллическом состоянии. Такие структуры очень чувствительны к изменению температуры, давления, химического состава и электродинамических характеристик окружения. По этой причине, при изменении внешних условий липиды мембраны могут испытывать локальные или генерализованные фазовые переходы I рода из жидкокристаллического в гель-состояние, которое иногда условно называют твердокристаллическим. Для переходов I рода характерно скачкообразное изменение внутренней энергии и плотности вещества. При этом возможно появление разных кристаллических модификаций. Это превращение обусловлен о сложными физическими свойствами фосфолипидов. В жидкокристаллическом состоянии бислой имеет меньшую толщину, меньшую вязкость, меньшую упорядоченность молекул, бóльшую ионную проводимость, бóльшую растворимость веществ, чем в твердом состоянии. Различна и конформация (структура) молекул в жидком и твердом состояниях. Это подтверждается данными рентгеноструктурного анализа. В жидкой фазе молекулы фосфолипидов имеют структуру октаэдров и могут образовывать полости («кинки»), которые способны перемещаться. Внедрившись в такую полость любые молекулы получают возможность диффундировать вместе с «кинком» по мембране.
Для исследования некоторых физических свойств биологических мембран используется метод флюоресцентного анализа. Сама мембрана в нормальном состоянии не флюоресцирует. Поэтому, при использовании этого метода, в мембрану необходимо вводить молекулы или молекулярные группы, способные к флюоресценции – флюоресцентные зонды и метки. С этой целью используют молекулы диметиламинохалкона (ДМХ), анилин-нафталин-сульфонат (АНС) и другие вещества. Флюоресцентный анализ дает возможность исследовать подвижность молекул в мембране, оценить вязкость липидной фазы (микровязкость) и некоторые другие свойства. Увеличение вязкости приводит к смещению спектра флюоресценции в область более коротких волн. Микровязкость можно оценить и по степени поляризации флюоресцентного излучения: Мембрана освещается полностью поляризованным светом. Излучение флюоресценции оказывается лишь частично поляризованным. Чем больше подвижность флюоресцирующей молекулы, тем меньше вязкость, тем меньше степень поляризации.
|
|
|
Наиболее полное представление об агрегатном состоянии липидных бислоев дают методы радиоспектроскопии – электронный парамагнитный резонанс (ЭПР) и ядерный магнитный резонанс (ЯМР).
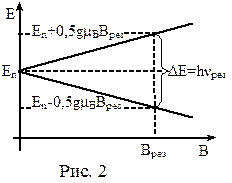 ЭПР – это явление резкого возрастания поглощения энергии электромагнитного излучения резонансной частоты νрез. системой парамагнитных частиц, помещённой в постоянное магнитное поле. Такие частицы обладают неспаренными электронами, а значит и нескомпенсированным магнитным моментом атома (например, свободные радикалы). Будучи помещёнными в постоянное магнитное поле, такие атомы испытывают расщепление энергетических уровней (рис.2). Переходы между уровнями соответствуют микроволновому диапазону электромагнитного излучения.
ЭПР – это явление резкого возрастания поглощения энергии электромагнитного излучения резонансной частоты νрез. системой парамагнитных частиц, помещённой в постоянное магнитное поле. Такие частицы обладают неспаренными электронами, а значит и нескомпенсированным магнитным моментом атома (например, свободные радикалы). Будучи помещёнными в постоянное магнитное поле, такие атомы испытывают расщепление энергетических уровней (рис.2). Переходы между уровнями соответствуют микроволновому диапазону электромагнитного излучения.
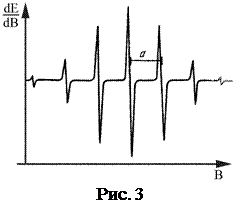 Спектром ЭПР называют зависимость энергии E, поглощённой исследуемым веществом, от величины индукции B магнитного поля (рис.3). Если в структуре электронных оболочек атомов неспаренные электроны отсутствуют, то для исследования таких веществ используют спин-метки и спин-зонды, обладающие такими электронами. Эти соединения вводят в изучаемую структуру в процессе химического синтеза. В качестве спин-меток и спин-зондов используют соединения, представляющие собой различные нитроксильные радикалы (
Спектром ЭПР называют зависимость энергии E, поглощённой исследуемым веществом, от величины индукции B магнитного поля (рис.3). Если в структуре электронных оболочек атомов неспаренные электроны отсутствуют, то для исследования таких веществ используют спин-метки и спин-зонды, обладающие такими электронами. Эти соединения вводят в изучаемую структуру в процессе химического синтеза. В качестве спин-меток и спин-зондов используют соединения, представляющие собой различные нитроксильные радикалы (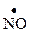 ), которые можно присоединить к любому атому углерода углеводородной цепочки молекул липидов. При этом метка замещает какую-либо группу, образуя с молекулой ковалентные связи. Соединения-зонды встраиваются в молекулы липидов и удерживаются там электростатическими или гидрофобными силами.
), которые можно присоединить к любому атому углерода углеводородной цепочки молекул липидов. При этом метка замещает какую-либо группу, образуя с молекулой ковалентные связи. Соединения-зонды встраиваются в молекулы липидов и удерживаются там электростатическими или гидрофобными силами.
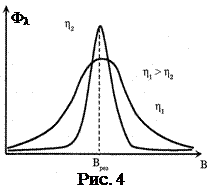 Применение ЭПР основано на том, что форма спектра (вид графика поглощения) зависит от свойств окружения зонда или метки, а в первую очередь от микровязкости среды (рис.4). По характеру изменения спектра ЭПР можно безошибочно обнаружить не только перемещения хвоста с присоединённой сигнальной группой, но и определить скорость латеральной диффузии (D ≈ 1,8·10-8 см2с-1). Было установлено, что скорость поперечного перемещения (флип-флоп) липидов в 103 раз меньше, чем латерального. В жидкокристаллической фазе жирнокислотные цепи фосфолипидов обладают значительно большей подвижностью, чем в твердой фазе. Методом ЭПР установлено снижение подвижности липидов при увеличении содержания холестерина, перекисном окислении и действии ряда лекарственных препаратов. Увеличение подвижности отмечено при тиреотоксикозах и ряде других патологий. Недостаток метода: внедрение зонда или метки изменяет химическую структуру молекул фосфолипидов.
Применение ЭПР основано на том, что форма спектра (вид графика поглощения) зависит от свойств окружения зонда или метки, а в первую очередь от микровязкости среды (рис.4). По характеру изменения спектра ЭПР можно безошибочно обнаружить не только перемещения хвоста с присоединённой сигнальной группой, но и определить скорость латеральной диффузии (D ≈ 1,8·10-8 см2с-1). Было установлено, что скорость поперечного перемещения (флип-флоп) липидов в 103 раз меньше, чем латерального. В жидкокристаллической фазе жирнокислотные цепи фосфолипидов обладают значительно большей подвижностью, чем в твердой фазе. Методом ЭПР установлено снижение подвижности липидов при увеличении содержания холестерина, перекисном окислении и действии ряда лекарственных препаратов. Увеличение подвижности отмечено при тиреотоксикозах и ряде других патологий. Недостаток метода: внедрение зонда или метки изменяет химическую структуру молекул фосфолипидов.
|
|
|
Этого недостатка лишён метод ядерного магнитного резонанса (ЯМР). Ядерный магнитный резонанс – это явление резкого возрастания поглощения энергии электромагнитных волн определённой частоты (νрез) системой парамагнитных ядер, помещенных в постоянное магнитное поле. Частота переменного электромагнитного поля νрез меньше, чем при ЭПР. В структуре биологических объектов содержится много водорода, ядра которого (протоны, 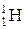 ) являются парамагнитными. Это дает возможность применять при изучении подвижности молекул фосфолипидов метод ЯМР.
) являются парамагнитными. Это дает возможность применять при изучении подвижности молекул фосфолипидов метод ЯМР.
 2014-02-09
2014-02-09 376
376






