Как следует из (1.4), H = 0 только в двух случаях:
1. какая-либо из вероятностей p(Aj) = 1; однако, при этом следует, что все остальные p(Ai) = 0 (i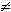 j), т.е. реализуется ситуация, когда один из исходов является достоверным (и общий итог опыта перестает быть случайным);
j), т.е. реализуется ситуация, когда один из исходов является достоверным (и общий итог опыта перестает быть случайным);
2. все вероятности p(Ai) = 0, т.е. никакие из рассматриваемых исходов опыта невозможны, поскольку нетрудно показать, что:
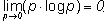
Во всех остальных случаях, очевидно, что H > 0.
Очевидным следствием свойства аддитивности (1.1) будет утверждение, что для двух независимых опытов  и
и 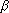
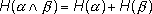 (1.5)
(1.5)
Энтропия сложного опыта, состоящего из нескольких независимых, равна сумме энтропий отдельных опытов.
Пусть имеется два опыта с одинаковым числом исходов n, но в одном случае они равновероятны, а в другом – нет. Каково соотношение энтропий опытов? Примем без доказательства следующее утверждение:
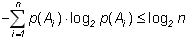 (1.7)
(1.7)
При прочих равных условиях наибольшую энтропию имеет опыт с равновероятными исходами.
Другими словами, энтропия максимальна в опытах, где все исходы равновероятны.
Здесь усматривается аналогия (имеющая глубинную первооснову!) с понятием энтропии, используемой в физике.
Впервые понятие энтропии было введено в 1865 г. немецким физиком Рудольфом Клаузиусом как функции состояния термодинамической системы, определяющей направленность самопроизвольных процессов в системе.
Клаузиус сформулировал II начало термодинамики. В частности, он показал, что энтропия достигает максимума в состоянии равновесия системы.
Позднее (в 1872 г.) Людвиг Больцман, развивая статистическую теорию, связал энтропию системы с вероятностью ее состояния, дал статистическое (вероятностное) толкование II-му началу термодинамики и, в частности, показал, что вероятность максимальна у полностью разупорядоченной (равновесной) системы, причем, энтропия и термодинамическая вероятность оказались связанными логарифмической зависимостью.
Другими словами, в физике энтропия оказывается мерой беспорядка в системе.
При этом беспорядок понимается как отсутствие знания о характеристиках объекта (например, координат и скорости молекулы); с ростом энтропии уменьшается порядок в системе, т.е. наших знания о ней.
Сходство понятий и соотношений между ними в теории информации и статистической термодинамике, как оказалось позднее, совершенно не случайно.
 2014-02-12
2014-02-12 547
547








