Швейцарский ученый И.Бальмер (1825-1898) подобрал эмпирическую формулу, описывающую спектральные линии атома водорода в видимой области спектра.
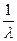 = R’ (
= R’ (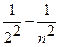 ), (n =3,4,5,...),
), (n =3,4,5,...),
где R’ = 1,10.107м-1 – постоянная Ридберга. Так как ν = c/λ, то
ν= R (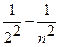 ), (n = 3,4,5,...),
), (n = 3,4,5,...),
где R = R’c = 3,29.1015 с-1 – также постоянная Ридберга. Спектральные линии, отличающиеся различными значениями n, образует группу или серию линий, называемую серией Бальмера. С увеличением n линии серии сближаются. Значения n = ¥ определяет границу серии, к которой со стороны больших частот примыкает сплошной спектр. В начале ХХ века в спектре атома водорода было обнаружено еще несколько серий. В ультрафиолетовой области – серия Лаймана:
ν= R (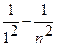 ), где n =2,3,4,...
), где n =2,3,4,...
В инфракрасной области:
Серия Пашена: ν= R (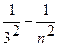 ), n = 4,5,6,...
), n = 4,5,6,...
Серия Брэкета ν= R (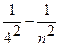 ), n = 5,6,7,...
), n = 5,6,7,...
Серия Пфунда ν= R (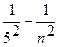 ), n = 6,7,8,...
), n = 6,7,8,...
Серия Хэмфри ν = R (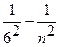 ), n = 7,8,9,...
), n = 7,8,9,...
Все приведенные выше серии могут быть описаны одной формулой
ν= R (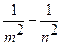 ), (212)
), (212)
где m имеет в каждой серии постоянное значение, m = 1,2,3,4,5,6 – определяет серию; n принимает целочисленные значения начиная с m +1 (определяет отдельные линии серии).
 2015-01-30
2015-01-30 716
716








