Согласно закону эквивалентов, молярные массы эквивалентов (эквивалентные объемы) реагирующих друг с другом веществ Мэк(1) и Мэк(2) пропорциональны их массам (объемам).
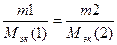 (1)
(1)
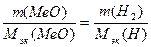 (2)
(2)
Если одно из веществ находится в газообразном состоянии, то, как правило, его количество измеряется в объемных единицах (см3; дм3; м3).
Объем, занимаемый при данных условиях, молярной массой или молярной массой эквивалента называется МОЛЯРНЫМ или, соответственно, эквивалентным объемом вещества. МОЛЯРНЫЙ объем любого газа при н.у. равен 22,4л. Отсюда эквивалентный объем водорода, молекула которого состоит из двух атомов, т.е. содержит два моль атома водорода, равен 22,4: 2 = 11,2 дм3.
По формуле (2) найдем число эквивалентов водорода через объемное соотношение
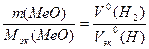 (3)
(3)
где V°(H2) - объем использованного на восстановление водорода, измеренный при н.у., дм3
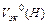 - эквивалентный объем водорода, дм3.
- эквивалентный объем водорода, дм3.
Из уравнения (3) находим эквивалентную массу оксида металла
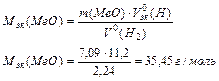
Согласно закону эквивалентов
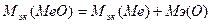
Отсюда
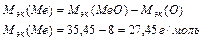
Так как металл имеет степень окисления +2, то
fэк =1/2,
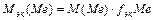
отсюда следует, что
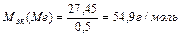
Так как атомная масса в а.е.м. численно равна мольной массе, выраженной в г/моль, то А(Ме) = 54,9 а.е.м.
 2015-01-30
2015-01-30 365
365








