Лабораторная работа № 1
Гравиметрическое определние кристаллизационной воды в хлориде бария
Цель работы. Определение воды в твердых веществах – один из наиболее важных случаев определения, так как вода нередко является основной частью анализируемых веществ. Содержание воды определяют как прямыми, так и косвенными методами.
Кристаллизационной называется вода, входящая в структуру кристаллов некоторых веществ, называемых кристаллогидратами. Содержание кристаллизационной воды в кристаллогидратах отвечает определенным химическим формулам, например ВаС12×2Н2О, CuSO4×5H2O, Na2SO4×10H2O, Na2SO4×7H2O и т. д. Вследствие этого кристаллизационную воду называют также стехиометрической водой.
При нагревании кристаллогидраты разлагаются с выделением воды. На этом основано определение содержания кристаллизационной воды в большинстве кристаллогидратов методом отгонки. Так, в рассматриваемом случае навеску ВаС12×2Н2О, помещенную в бюкс, нагревают до 120 – 125 °С в сушильном шкафу до тех пор, пока не перестанет изменяться масса вещества (высушивание до постоянной массы).
Достижение постоянной массы свидетельствует, очевидно, о том, что вся кристаллизационная вода уже удалена. Масса ее равна убыли в массе вещества.
Приборы и реактивы. Сушильный шкаф; технические весы; аналитические весы; эксикатор; тигельные щипцы; стеклянный бюкс; хлорид бария кристаллический, BaCl2×2H2O.
Выполнение работы.
Взятие навески.
1. Тщательно вымытый бюкс высушивают в сушильном шкафу и, не закрывая крышкой, охлаждают, поставив на 20 мин в эксикатор около весов.
2. После этого, соблюдая все правила, точно взвешивают бюкс вместе с крышкой на аналитических весах. Затем помещают в него около 1,5 г свежеперекристаллизованного ВаС12×2Н2О и, закрыв крышкой, снова точно взвешивают.
Высушивание.
1. Открыв бюкс, помещают крышку сверху бюкса боком (т. е. перевернув на ребро) и ставят на полку (не на дно) сушильного шкафа. Под бюкс следует подложить листок бумаги с указанием своей фамилии. Выдерживают бюкс в шкафу при температуре около 125 °С приблизительно 2 ч. Затем тигельными щипцами переносят бюкс и крышку его в эксикатор.
2. Продержав эксикатор 20 мин около весов, вынимают из него бюкс и, закрыв крышкой, точно взвешивают. Далее снова ставят бюкс с веществом в сушильный шкаф и выдерживают его там (открыв крышку) еще около 1 ч, повторно охлаждают в эксикаторе и снова взвешивают.
3. Если второе взвешивание дает тот же самый результат, что и первое, или отличается от него не более чем на 0,0002 г, кристаллизационную воду можно считать удаленной практически полностью. В противном случае высушивание с периодическим взвешиванием повторяют до тех пор, пока не будет достигнуто постоянство массы. Результаты всех повторных взвешиваний обязательно записывают в лабораторный журнал, даже если они одинаковые.
Если работу приходится прерывать, бюкс оставляют в эксикаторе.
Таблица. Результаты определения кристаллизационной воды
| Масса бюкса с веществом, г | 9,5895 |
| Масса бюкса, г | 8,1320 |
| Навеска ВаС12×2Н2О, m(ВаС12×2Н2О), г | 1,4575 |
| Масса бюкса с веществом после высушивания 1-е взвешивание, г | 9,3747 |
| 2-е взвешивание, г | 9,3749 |
Расчеты.
Масса кристаллизационной воды в навеске:
m(H2O) = 9,5895 - 9,3748 = 0,2147 г
Массовая доля кристаллизационной воды в ВаС12×2Н2О вычисляют из пропорции:
в 1,4575 г ВаС12×2Н2О содержится 0,2147 г Н2О
в 100 г ВаС12×2Н2О – х г Н2О
 %
%
Расчет ошибки определения. Для проверки найденную величину сравнивают с теоретически вычисленным значением массовой доли Н2О в ВаС12×2Н2О.
В 1 моль (244,3 г) ВаС12×2Н2О содержится 2 моль воды, т.е. 36,03 г Н2О.
Составим пропорцию:
в 244,3 г ВаС12×2Н2О содержится 36,03 г Н2О
в 100 г ВаС12×2Н2О – х г Н2О
 %
%
Абсолютная ошибка составляет:
d = 14,73% – 14,75% = –0,02%.
Относительную ошибку определения вычисляют по формуле
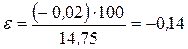 %
%
Эта погрешность объясняется ошибками взвешивания. При правильной работе абсолютная ошибка данного определения не должна превышать ±0,05%. Другими словами, приемлемы результаты, лежащие в пределах от 14,70 до 14,80%.
Лабораторная работа № 2
Гравиметрическое определение сульфатов в виде сульфата бария
Метод основан на осаждении сульфат-ионов в виде кристаллического белого осадка BaSO4 и получении гравиметрической формы (BaSO4) прокаливанием:
SO42– + Ba2+ = BaSO4
Данным методом определяют сульфатную серу, а также свободную, пиритную и сульфидную, предварительно окислив их до сульфатной.
Осаждению сульфат-ионов в виде BaSO4 мешают анионы SiO32–, SnO32–, WO42– и другие, образующие осадки соответствующих кислот при подкислении раствора. Осаждению мешают также ионы Fe3+, Al3+, С1–, МпО4– и другие, соосаждаемые с BaSO4. Мешающие ионы должны быть предварительно удалены из анализируемого раствора.
Приборы и реактивы. Муфельная печь; аналитические весы; водяная или песчаная баня; эксикатор; стеклянные палочки; стеклянные воронки; фарфоровые тигли; мерный цилиндр вместимостью 100 мл; щипцы тигельные; химические стаканы вместимостью 200 – 250 и 100 мл; фильтры беззольные «синяя лента»; хлорид бария, 3 М раствор; хлороводородная кислота, 6 М раствор.
 2015-01-30
2015-01-30 2495
2495







