1. Реакция «серебряного зеркала»
В чистую пробирку внести 2 капли аммиачного раствора оксида серебра, прибавить
1 каплю раствора формалина и смесь осторожно нагреть на водяной бане при
60 – 70 0С. Через несколько минут на стенках пробирки выделяется слой металлического серебра в виде зеркала или появляется черный осадок металлического серебра:
|
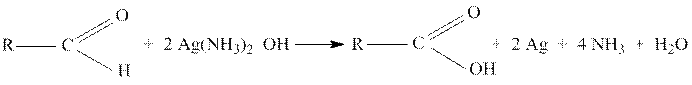
Примечание. Формалин – водный раствор, содержащий 40% формальдегида,
8% метанола и 52% воды. Источник формальдегида.
.
2. Восстановление альдегидами гидроксида меди (II)
В пробирку наливают 0,5 мл формалина или уксусного альдегида, 3 – 4 мл 2 н. раствора гидроксида натрия и по каплям добавляют раствор медного купороса до появления мути. При нагревании верхней части пробирки наблюдается появление желтого осадка, переходящего в красный, при образовании оксида меди (I):
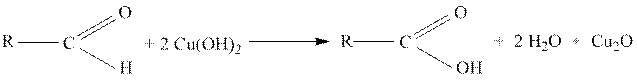
3. Окисление альдегидов реактивом Фелинга
В пробирку налить 0,5 – 1 мл реактива Фелинга и 4 – 5 капель формалина. Осторожно нагреть верхнюю часть пробирки. Раствор окрашивается в оранжево-красный цвет гидроксида меди (I), который переходит в красный осадок оксида меди (I). Химизм этого процесса аналогичен опыту 2.
Примечание. Реактив Фелинга (жидкость Фелинга):
раствор CuSO4 и тартрата калия-натрия
в 10%-ном растворе гидроксида натрия
(CuSO4+KNaC4H4O6+(10% NaOH+90% H2O).
4. Окисление альдегидов перманганатом калия
В пробирку прилить 1 мл формальдегида, добавить 0,5 мл раствора перманганата калия, подкисленного серной кислотой. Содержимое пробирки встряхивают.
 2015-01-07
2015-01-07 1477
1477








