Спектр атома водорода отличается своей простотой и ясностью. Простота спектра объясняется простотой структуры атома водорода, состоящего из ядра (один протон) и одного электрона, движущегося в поле протона.
Совокупность волновых чисел линий, лежащих в видимой части спектра, может быть описана с помощью уравнения:
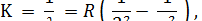
где R - постоянная, одинаковая для всех линий, равная R=109677 см, получила название постоянной Ридберга, n = 3, 4, 5....Это соотношение известно как формула Бальмера, группа линий в спектре атома водорода, охватываемая этой формулой, соответственно - серия Бальмера.
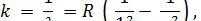
где n = 2,3,4.... Эта группа линий была открыта Лайманом в 1906 году и получила название серии Лаймана. Позднее были найдены серии в инфракрасной области:
Серия Пашена (1908 г).
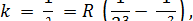
n = 4,5,6,
Серия Брекетта (1922 г).
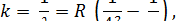
n = 5,6, 7,...
Все серии линий атома водорода могут быть выражены одной формулой:
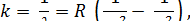
где n 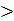 m и n, m - целые числа, m = const для данной серии. Это выражение часто называют обобщенной формулой Бальмера.
m и n, m - целые числа, m = const для данной серии. Это выражение часто называют обобщенной формулой Бальмера.
 2015-01-07
2015-01-07 302
302







