Фотоколориметрическое определение содержания железа основано на образовании окрашенных комплексов железа с сульфосалициловой кислотой. В слабокислой среде (рН > 4) сульфосалициловая кислота взаимодействует только с ионами Fe3+ образуя комплекс красного цвета, устойчивый при рН 4-8. В щелочной среде (рН 8-11,5) сульфосалициловая кислота реагирует с ионами Fe3+ и Fe2+, образуя комплекс жёлтого цвета. Содержание Fe2+ находят по разности.
Материалы и оборудование: ФЭК, мерные колбы вместимостью 50 и 100 см3; конические колбы на 50 см3; пипетки на 1, 2, 5 и 20 см3.
Реактивы: Хлорид аммония, сульфасалициловая кислота, раствор аммиака (1:1), стандартный раствор железа.
Ход анализа. Отбирают 15 см3 анализируемого фильтрата или раствора, полученного при растворении зольного остатка, помещают в мерную колбу вместимостью 25 см3. К пробе приливают раствор аммиака (1:1) до нейтрализации (рН = 7) (по индикаторной бумаге), приливают 2 см3 хлорида аммония, 2 см3 сульфосалициловой кислоты или сульфосалицилата натрия, 2 см3 раствора аммиака 1:1. Доводят до метки дистиллированной водой. Через 5 мин измеряют оптическую плотность при длине волны 425 нм с соответствующим светофильтром относительно холостого раствора на дистиллированной воде.
|
|
|
По оптической плотности на калибровочном графике находят содержание железа в растворе.
Концентрацию железа (С, мг/г сухих листьев) в анализируемой пробе вычисляют по формуле
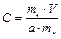 ,
,
где 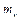 - количество железа, определённое по калибровочному графику, мг;
- количество железа, определённое по калибровочному графику, мг;
а - аликвотная часть исследуемого раствора, взятая для анализа из общего объёма, см3;
V - общий объём анализируемого раствора, см3;
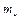 - масса навески листьев, взятая для анализа, г.
- масса навески листьев, взятая для анализа, г.
Полученные результаты сравнивают с результатами фоновой пробы и делают вывод о состоянии окружающей среды на различных территориях, представленных анализируемыми пробами.
 2015-02-27
2015-02-27 1016
1016








