310. Увеличение радиуса атома происходит в ряду:
А) Литий→ бериллий→ бор
В) Натрий → магний → алюминий
С) Углерод → азот → кислород
D) Литий → натрий → калий
E) Кремний → фосфор → сера
311. Уменьшение электроотрицательности элемента происходит в ряду:
А) Литий→ бериллий→ бор
В) Натрий → магний → алюминий
С) Углерод → азот → кислород
D) Литий → натрий → калий
E) Кремний → фосфор → сера
312. В главных подгруппах периодической системы сверху вниз у элементов:
А) Уменьшается радиус атома
В) Увеличивается радиус атома
С) Увеличивается электроотрицательность
D) Увеличивается энергия ионизации
Е) Затрудняется отрыв электрона от атома
313.Элементы главных подгрупп периодической системы – это:
А) d- и f-элементы
В) s- и p-элементы
С) d-элементы
D) f-элементы
Е) s- и d –элементы
314. В главных подгруппах периодической системы сверху вниз у элементов:
А) Ослабевают металлические свойства
В) Усиливаются неметаллические свойства
С) Ослабевают неметаллические свойства
D) Способность атома к отдаче электронов затрудняется
Е) Радиус атома уменьшается
315. У элементов главных подгрупп все валентные электроны атома располагаются на:
А) (n-1) d-подуровне
В) (n-1) s- подуровне
С) (n-1) р- подуровне
D) n d- и n f- подуровне
Е) n s- и n р- подуровне
316. У элементов IА и IIА групп периодической системы все валентные электроны атома располагаются на:
А) n р-подуровне
В) (n-1) s-подуровне
С) (n-1) р-подуровне
D) n f-подуровне
Е) n s-подуровне
317. Водородные соединения элементов IА и IIА групп периодической системы являются соединениями характера:
А) Ковалентного
В) Металлического
С) Кислотного
D) Ионного
Е) Амфотерного
318. Водородные соединения элементов IА и IIА групп периодической системы являются соединениями характера:
А) Кислотного
В) Основного
С) Амфотерного
D) Ковалентного
Е) Металлического
319. У гидроксидов элементов главных подгрупп сверху вниз по подгруппе при постоянстве заряда иона элемента:
А) Усиливаются основные свойства
В) Усиливаются кислотные свойства
С) Ослабевают основные свойства
D) Усиливается способность диссоциировать с образованием Н+-ионов
Е) Ослабевает способность диссоциировать с образованием ОН−-ионов
320. В ряду Li → Na → K → Rb → Cs → Fr от лития к францию:
А) Уменьшается радиус атома
В) Увеличивается энергия ионизации
С) Увеличивается радиус атома
D) Увеличивается электроотрицательность
Е) Уменьшаются металлические свойства
321. В подгруппе F → Cl → Br → I от фтора к иоду:
А) Уменьшается радиус атома
В) Увеличивается энергия ионизации
С) Увеличивается электроотрицательность
D) Уменьшается электроотрицательность
Е) Усиливаются неметаллические свойства
322. С увеличением порядкового номера у гидроксидов элементов IIА группы:
А) Уменьшается растворимость
В) Уменьшаются основные свойства
С) Усиливаются основные свойства
D) Усиливаются амфотерные свойства
Е) Усиливаются кислотные свойства
323. Периоды периодической системы, в которых расположены элементы только главных подгрупп:
А) I, II, III
B) I, III, IV
C) II, III, IV
D) III, IV, V
E) II, IV, V
324. Ядро атома криптона – 80, 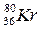 содержит:
содержит:
A) 80p и 36n;
B) 36p и 44е;
C) 36р и 80n;
D) 36р и 44n;
E) 44р и 44n.
325. Элемент, обнаруженный на Солнце, раньше чем на Земле:
A) Аргон;
B) Калий;
C) Гелий;
D) Радон;
E) Криптон.
326. Самый легкий газ после водорода:
A) Азот;
B) Неон;
C) Озон;
D) Гелий;
E) Аргон.
327. Низшая степень окисления ксенона в соединениях:
A) +2;
B) +4;
C) +8;
D) +6;
E) +5.
328. Наиболее распространенный после водорода элемент Космоса:
А) Гелий
В) Неон
С) Аргон
D) Криптон
Е) Ксенон
329. Ксенон непосредственно реагирует только с:
А) Кислородом
В) Хлором
С) Фтором
D) Водородом
Е) Озоном
 2015-02-04
2015-02-04 423
423








