Раздел химической термодинамики, занимающийся изучением теплот реакций, называется термохимией.
В химических процессах изменение состояния системы может характеризоваться не двумя, как в технической термодинамике, а тремя и более параметрами (например, давлением, удельным объемом, температурой, концентрацией). При этом в процессе изменения состояния могут оставаться постоянными два параметра.
Как правило, рассматривают два вида реакций:
а) изохорно-изотермическую, то есть при (V, T) = const;
б) изобарно-изотермическую, то есть при (p, T) = const.
Изохорно-изотермические реакции протекают между твердыми и жидкими веществами, между газами в постоянном объеме (в нерасширяющемся сосуде или для очень быстро протекающих реакций, типа взрыва, когда за время реакции вещества не успевают расшириться). Изобарно-изотермические реакции протекают достаточно медленно в условиях постоянного давления.
Для изохорно-изотермической реакции:
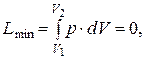
тогда
Q V max = D U,
где Q V max – теплота изохорно-изотермической реакции.
Для изобарно-изотермической реакции:
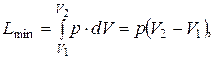
тогда
–D U = – Q p max + p (V 2 – V 1),
где Q p max – теплота изобарно-изотермической реакции.
Q p max = D U + p (V 2 – V 1) = U 2 – U 1 + pV 2 – pV 1 =
= (U 2 + pV 2 ) – (U 1 + pV 1) = I 2 – I 1.
Таким образом,
Q p max = D I.
Связь между тепловыми эффектами при изохорно-изотермической и изобарно-изотермической реакциями:
Q V max = Q p max – p (V 2 – V 1),
Если в реакции участвуют газообразные вещества, то из уравнения состояния идеального газа
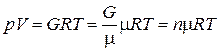
где n – число молей в объеме V;
m R – универсальная газовая постоянная.
Отсюда
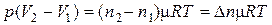 .
.
Тогда
Q V max = Q p max – D n m RT = Q p max – 8,3143D nT [кДж/моль].
Пусть D n > 0, например, в реакции горения жидкого бензола:
C6H6(ж) + 7,5O2(г) = 6CO2(г) + 3H2O(г) – 3259000 [кДж/моль]
Количество молей газообразных продуктов:
n 1 = 7,5 моль, n 2 = 9 моль, D n = 1,5 моль, следовательно:
Q V max < Q p max,
то есть при изохорно-изотермической реакции тепла выделится больше, чем при изобарно-изотермической, так как в последнем случае, чтобы p = const, система совершит работу расширения.
Если D n < 0:
CO(г) + 0,5O2(г) = CO2(г) – 28330 [кДж/моль]
n 1 = 1,5 моль, n 2 = 1 моль, Dn = – 0,5 моль, – таким образом, работа расширения
p (V 2 – V 1) < 0,
то есть
Q V max > Q p max.
В данном случае при изохорно-изотермической реакции тепла выделится меньше, чем при изобарно-изотермической, так как для поддержания p = const система воспринимает работу, совершаемую внешней средой.
Если число молей газообразных продуктов в реакции остается неизменным D n = 0, то
Q V max = Q p max.
В справочной литературе чаще встречаются значения Qp. Для взрывчатых веществ есть таблицы значений QV. Это теплоты образования веществ из простых веществ. Хотя индекс «max» не указан, это именно максимальные тепловые эффекты.
 2015-03-07
2015-03-07 565
565








