Некоторые соли, образованные очень слабым основанием и слабой летучей кислотой (Cr2S3, Al2S3, Cr2(CO3)3, Fe2(CO3)3, Al2(CO3)3 и др.), при нагревании в присутствии воды подвергаются полному необратимому гидролизу. При этом образуются слабо диссоциирующие основание и кислота. Оба продукта уходят из сферы реакции в виде осадков и газов. Аналогично гидролизуются смеси солей, одна из которых образована очень слабым основанием и сильной кислотой, а другая – сильным основанием и слабой летучей кислотой (Na2S + CrCl3, Na2CO3 + Al2(SO4)3 и т.п.). Например:
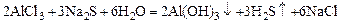 .
.
Выполнение опыта. В две пробирки внести по 5 – 10 капель 1М растворов: в одну – хлорида или сульфата хрома, в другую – хлорида (или сульфата) алюминия. В первую пробирку прибавить раствор сульфида натрия, во вторую - раствор карбоната натрия до выпадения осадков малорастворимых соединений. Отметить выделение газа. Какие это газы?
Написать уравнения гидролиза смесей солей в молекулярном и ионном виде. Доказать, что в осадке гидроксиды, а не сульфид хрома или карбонат алюминия. Для этого слить растворы с полученных осадков, разделить каждый из осадков на две пробирки, в одну из них добавить раствор щелочи, а в другую раствор кислоты. Наблюдать растворение осадков во всех пробирках. Объяснить наблюдаемые процессы. Почему при взаимодействии растворов этих солей гидролиз протекает практически необратимо? Каков механизм взаимного усиления гидролиза?
|
|
|
 2015-04-01
2015-04-01 618
618








