Задача 10-1 (автор Куриленко К. А.)
1. На основании того, что соль A имеет интенсивно-синюю окраску и образуется из растворов солей железа и цианида калия, можно предположить, что она является цианидным комплексом железа – Fe4[Fe(CN)6]3 (берлинская лазурь). Эта краска в 18 веке широко использовалась в красильном деле и книгопечатании. Исходя из этого предположения, можно определить состав соли В, она может содержать ионы калия и анионы:[Fe(CN)6]3− или [Fe(CN)6]4−
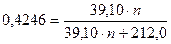 ;
;
где n – количество атомов калия в B,
решая уравнение, находим n = 4, откуда B – K4[Fe(CN)6].
A − Fe4[Fe(CN)6]3 или KFe[Fe(CN)6] (берлинская лазурь, железная лазурь, парижская лазурь, прусская лазурь, гамбургская синь);
B – K4[Fe(CN)6] (желтая кровяная соль, желтое синькали).
2. При прокаливании железа с серой образуется сульфид железа,
Fe + S → FeS (реакция 1)
который взаимодействует с цианидом калия, образуя желтую кровяную соль;
6KCN + FeS → K4[Fe(CN)6] + K2S (реакция 2);
если же к полученному после растворения в воде раствору K4[Fe(CN)6] добавить подкисленный раствор железного купороса на воздухе, то будет выделяться осадок берлинской лазури;
3K4[Fe(CN)6] + 12FeSO4 + 3O2 +6H2SO4 → Fe4[Fe(CN)6]3 +4Fe2(SO4)3 +6K2SO4 + 6H2O
(реакция 3).
Fe4[Fe(CN)6]3 разлагается под действием щелочей с выделением гидратированного оксида железа Fe2O3∙ n H2O;
Fe4[Fe(CN)6]3 + 12KOH → 2Fe2O3∙ n H2O + 3K4[Fe(CN)6] + (6 – 2 n)H2O (реакция 4).
3. Метод получения берлинской лазури, описанный Д. Вудвордом, заключает в себе ряд недостатков, так при прокаливании органических остатков (кожа, шерсть) большое количество азота теряется в виде аммиака, синильной кислоты, летучих органических соединений, и лишь 10 – 15 % переходит в KCN, поэтому сейчас используют другие способы получения цианида калия.
а) 2CH4 + 3O2 + 2NH3 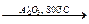 2HCN + 6H2O; HCN + KOH ® KCN + H2O.
2HCN + 6H2O; HCN + KOH ® KCN + H2O.
б) CaC2 + N2 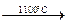 CaCN2 + C; CaCN2 + C + K2CO3
CaCN2 + C; CaCN2 + C + K2CO3 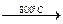 2KCN + CaCO3.
2KCN + CaCO3.
в) K2CO3 + 2NH3 + C 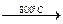 2KCN + 3H2O.
2KCN + 3H2O.
4. При взаимодействии желтой кровяной соли K4[Fe(CN)6] с хлором протекает окислительно-восстановительная реакция, в которой железо изменяет степень окисления с +2 на +3. В результате этого образуется другая комплексная соль калия – K3[Fe(CN)6] (соль С).
Исходя из данных, можно посчитать состав соли D;
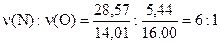 ;
;
по этому соотношению можно судить, что в соли D содержится один атом кислорода. Тогда
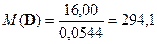 ;
;
Учитывая то, что цианокомплексы железа довольно устойчивы, можно предположить, что D содержит, кроме кислорода и азота, еще атомы железа, углерода и калия. Из вышесказанного следует, что анион соли D содержит центральный атом железа, 5 координированных цианид-ионов и, возможно, нитрозогруппу NO+. Тогда получаем
M (катиона) = 294,1 − 5∙ M (CN) – M (NO) − M (Fe) = 294,1 − 5∙26,02 – 30,01 − 55,85 = 78,14
Эта молярная масса соответствует 2 атомам калия, значит соль D – K2[Fe(NO)(CN)5].
C − K3[Fe(CN)6] (красная кровяная соль, красное синькали);
D – K2[Fe(NO)(CN)5] (нитропруссид калия).
5. При окислении K4[Fe(CN)6] хлором образуется красная кровяная соль по уравнению
2K4[Fe(CN)6] + Cl2 → 2K3[Fe(CN)6] + 2KCl (реакция 5);
если же обрабатывать желтую кровяную соль концентрированной азотной кислотой, то образуется K2[Fe(NO)(CN)5]
5K4[Fe(CN)6] + 18HNO3 → 5K2[Fe(NO)(CN)5] + 4N2 + 5CO2 + 10KNO3 + 9H2O
(реакция 6).
Система оценивания:
1. Формулы солей А и В 2 балла ´ 2 = 4 балла;
Подтверждение расчетом соли B 0,5 балла;
Названия А и В 1 балл ´ 2 = 2 балла;
2. Уравнения реакций 1–4 1 балл ´ 4 = 4 балла;
3. Способ получения KCN 1 балл;
4. Формулы солей С и D 2 балла ´ 2 = 4 балла;
Подтверждение расчетом соли D 0,5 балла;
Названия C и D 1 балл ´ 2 = 2 балла;
5. Уравнения реакций 5–6 1 балл ´ 2 = 2 балла;
Итого 20 баллов.
 2015-04-12
2015-04-12 501
501








