1. Элемент, содержащийся в большом количестве в рыбе, играющий важнейшую роль в процессах жизнедеятельности всех живых организмов, составляющий существенную часть костной ткани и зубной эмали человека, входящий в состав многих минеральных удобрений – фосфор (элемент Х).
Основным промышленным способом получения фосфора является высокотемпературное прокаливание в электрических печах смеси фосфорита (минерал В – Ca3(PO4)2, или точнее Ca10(PO4)6(OH)2 – гидроксиапатит), угля и кварцевого песка. Образующиеся при этом пары белого фосфора (Р4) конденсируют под слоем воды:
2Ca3(PO4)2 + 6SiO2 + 10C 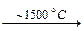 6CaSiO3 + 10CO + P4.
6CaSiO3 + 10CO + P4.
2. Рассчитаем молярную массу соединения А:
M = 4,28 ∙ 29 = 124,12 г/моль. Такая масса соответствует молекуле P4 .
Рассчитаем молярную массу соединения при температуре 900 °С:
M = 2,14 ∙ 29 = 62,06 г/моль. Такая масса соответствует молекуле P2.
3. Молекула Р4 представляет собой тетраэдр, в вершинах которого находятся атомы фосфора.
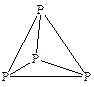
4. При нагревании белого фосфора с концентрированным раствором гидроксида бария образуется гипофосфит бария (соль С) и фосфин (соединение D), который вспыхивает на воздухе за счет небольшой примеси дифосфина (газа E):
2P4 + 3Ba(OH)2 + 6H2O ® 3Ba(H2PO2)2 + 2PH3.
2P2H4 + 7O2 ® 4HPO3 + 2H2O.
5. Графические формулы молекул фосфина, дифосфина и фосфорноватистой кислоты (F), образующейся при подкислении серной кислотой раствора гипофосфита бария:
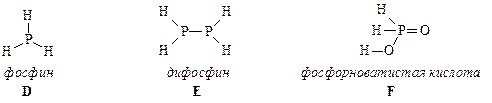 .
.
Фосфорноватистая кислота – кислота одноосновная: H3PO2 ⇄ H+ + H2PO2-. Запишем выражение для константы диссоциации этой кислоты:
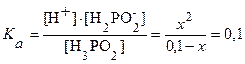 .
.
Решая полученное квадратное уравнение, получаем х = [H+]» 0,06 М.
Система оценивания:
1. Элемент Х 2 балла;
Уравнение реакции получения А 2 балла;
2. Расчет молярной массы при 400 °С и 900 °С по 0,5 балла
Формулы соединений по 0,5 балла
3. Структурная формула молекулы А 2 балла;
4. Уравнения реакций А с Ba(OH)2 и горения E 2 балла ´ 2 = 4 балла;
5. Структурные формулы D, E и F 2 балла ´ 3 = 6 баллов;
6. Расчет концентрации Н+ 2 балла;
Итого 20 баллов.
 2015-04-12
2015-04-12 890
890








