Процесс диссоциации слабых электролитов является обратимым. В системе устанавливается динамическое равновесие, которое может быть количественно оценено константой равновесия, выраженной через концентрации образующихся ионов и непродиссоциировавших молекул. Эта константа называется константой диссоциации. Для некоторого слабого электролита, распадающегося в растворе на ионы в соответствии с уравнением:
АaВb = aАx- + bВy+
константа диссоциации выразится следующим соотношением:
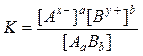 (63)
(63)
Для бинарного (распадающегося на два иона) электролита выражение (63) можно переписать в виде (63а):
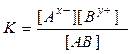 (63а)
(63а)
Поскольку концентрация каждого иона для бинарного электролита равна произведению степени диссоциации α на общую концентрацию электролита С, выражение (63а) в этом случае можно переписать следующим образом:
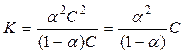 (64)
(64)
Для разбавленных растворов можно считать, что (1 – α) = 1. Тогда получаем:
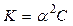
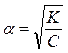 (65)
(65)
Таким образом, степень диссоциации слабого электролита обратно пропорциональна концентрации, т.е. прямо пропорциональна разбавлению раствора. Выражение (65) называют законом разбавления Оствальда.
Степень диссоциации слабого электролита можно связать с изотоническим коэффициентом i. Будем считать, что из N молекул электролита продиссоциировало n молекул, образовав νn ионов (ν – число ионов, на которые диссоциирует молекула). Поскольку изотонический коэффициент показывает, во сколько раз общее число молекул и ионов в растворе больше числа молекул до диссоциации, получаем:
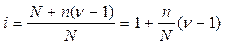
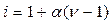 (66)
(66)
Соотношение (66) дает возможность, экспериментально определив изотонический коэффициент раствора, рассчитать степень диссоциации слабого электролита.
 2015-04-01
2015-04-01 417
417








