Закон Рауля: ”парциальное давление компонента идеального раствора равно произведению давления насыщенных паров при данной температуре на мольную долю компонента в жидкой фазе”
для НКК - 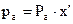
для ВКК - 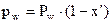
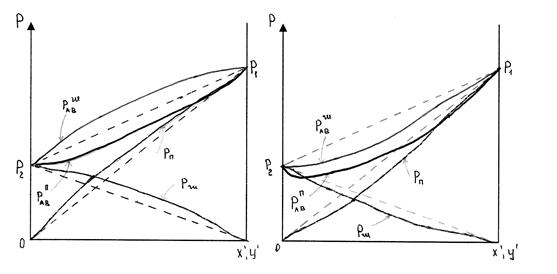
Положительное отклонение будет тогда, когда парциальные давления и общее давление системы будет больше величин, вычисленных по закону Рауля. На диаграммах кривая равновесия фаз и изобарно-температурные кривые выглядят так же как для идеального раствора (температуры кипящей жидкости и нас.паров повышаются с уменьшением концентрации НКК в жидкости и паре). КРФ характеризуется тем, что концентрация НКК в паровой фазе выше, чем в жидкости при любом составе жидкой фазы.
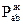 - изотерма жидкой фазы,
- изотерма жидкой фазы, 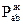 - изотерма паровой фазы,
- изотерма паровой фазы, 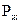 - парциальное давление ж.ф,
- парциальное давление ж.ф, 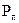 - парц.давление п.ф.
- парц.давление п.ф.
Отрицательное отклонение будет тогда, когда парциальные давления и общее давление системы будет меньше величин, вычисленных по закону Рауля.
Коэффициент активности характеризует степень данного раствора от идеального. 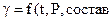 жидкости).
жидкости).
|
|
|
Закон Рауля с учетом γ: для НКК 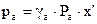 и для ВКК
и для ВКК 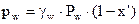 .
.
Состав равновесной жидкости: 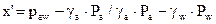 .
.
Состав равновесного пара: 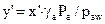
При положит.откл γ>1, а при отрицат.откл γ<1.
 2015-05-05
2015-05-05 960
960








