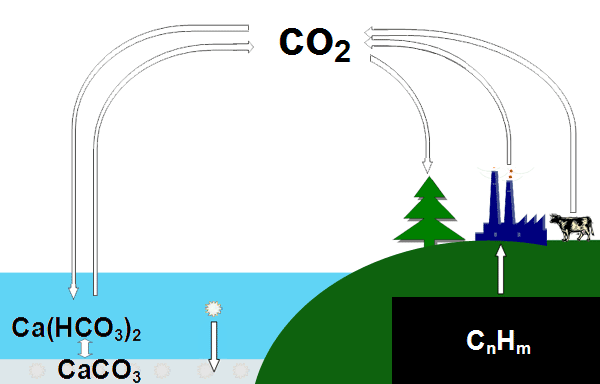
Если попросят написать уравнения, можно привести суммарное уравнение образования глюкозы при фотосинтезе:
6CO2 + 6H2O → C6H12O6 + 6O2
Сжигание метана в составе природного газа:
CH4 + 2O2 = CO2 + 2H2O
Обжиг известняка:
CaCO3 = CaO + CO2↑
Задача. Вычисление объема газа, вступившего в реакцию, если известна масса одного из продуктов реакции.
Пример:
2. Сколько литров водорода сгорело, если образовалось 72 г воды?
Решение:
- M (H2O) = 1 • 2 + 16 = 18 г/моль
- Находим количество вещества воды по условию задачи:
n = m / M = 72 г: 18 г/моль = 4 моль - Записываем над уравнением реакции имеющиеся данные, а под уравнением – число моль согласно уравнению (равно коэффициенту перед веществом):
x моль 4 моль
2H2 + O2 = 2H2O
2 моль 2 моль - Составляем пропорцию:
x моль – 4 моль
2 моль – 2 моль
Находим x:
x = 4 моль • 2 моль / 2 моль = 4 моль - Находим объем водорода:
v = 22,4 л/моль • 4 моль = 89,6 л
Ответ: 89,6 л.
Можно подставлять над и под уравнением непосредственно массу и объем веществ:
x л 72 г
2H2 + O2 = 2H2O
44,8 л 36 г
Билет № 24
 2015-04-20
2015-04-20 1151
1151







