Соединения с несколькими асимметрическими атомами обладают важными особенностями, отличающими их от рассмотренных ранее более простых оптически активных веществ с одним центром асимметрии.
Допустим, что в молекуле некоего вещества имеются два асимметрических атома; обозначим их условно А и Б. Легко видеть, что возможны молекулы со следующими комбинациями:
| (-) | (-) | (-) | (+) | ||
| Молекула 1 | А | Б | Молекула 3 | А | Б |
| (+) | (+) | (+) | (-) | ||
| Молекула 2 | А | Б | Молекула 4 | А | Б |
Молекулы 1 и 2 представляют собой пару оптических антиподов; то же самое относится и к паре молекул 3 и 4. Если же сравнивать друг с другом молекулы из разных пар антиподов - 1 и 3, 1 и 4, 2 и 3, 2 и 4, то мы увидим, что перечисленные пары не являются оптическими антиподами: конфигурация одного асимметрического атома у них совпадает, конфигурация другого - не совпадает. Это пары диастереомеров, т.е. пространственных изомеров, не составляющих друг с другом оптических антиподов.
Диастереомеры отличаются друг от друга не только оптическим вращением, но и всеми другими физическими константами: у них разные температуры плавления и кипения, разные растворимости и др. Различия в свойствах диастереомеров зачастую ничуть не меньше, чем различия в свойствах между структурными изомерами.
Примером соединения рассматриваемого типа может случить хлоряблочная кислота.
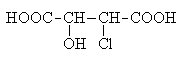
Ее стереоизомерные формы имеют следующие проекционные формулы:
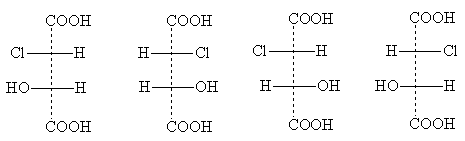
| эритро-формы | трео-формы |
Названия эритро - и трео - происходят от названий углеводов эритрозы и треозы. Эти названия употребляют для указания взаимного положения заместителей у соединений с двумя асимметрическими атомами: эритро -изомерами называют те, у которых два одинаковых боковых заместителя стоят в стандартной проекционной формуле на одной стороне (справа или слева); трео -изомерыимеют одинаковые боковые заместители на разных сторонах проекционной формулы. Два эритро- изомера представляют собой пару оптических антиподов, при их смешении образуется рацемат. Парой оптических изомеров являются и трео- формы; они тоже дают при смешении рацемат, отличающийся по свойствам от рацемата эритро- формы. Таким образом, всего существуют четыре оптически активных изомера хлоряблочной кислоты и два рацемата.
При дальнейшем росте числа асимметрических центров число пространственных изомеров возрастает, причем каждый новый асимметрический центр вдвое увеличивает число изомеров. Оно определяется формулой 2n, где n - число асимметрических центров.
Число стереоизомеров может уменьшаться из-за частичной симметрии, появляющейся в некоторых структурах. Примером может служить винная кислота, у которой число индивидуальных стереоизомеров сокращается до трех. Их проекционные формулы:
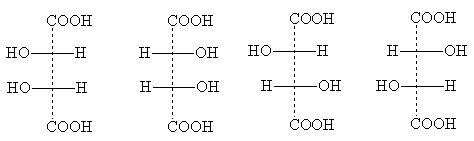
| I | Iа | II | III |
Формула I идентична с формулой Iа, так как превращается в нее при повороте на 180о в плоскости чертежа и, следовательно, не изображает нового стереоизомера. Это оптически неактивная модификация называется мезо-форма. Мезо-формы имеются у всех оптически активных веществ с несколькими одинаковыми (т.е. связанными с одинаковыми заместителями) асимметрическими центрами. Проекционные формулы мезо-форм всегда можно узнать по тому, что их можно разделить горизонтальной линией на две половины, которые по записи на бумаге формально идентичны, в действительности же зеркальны:
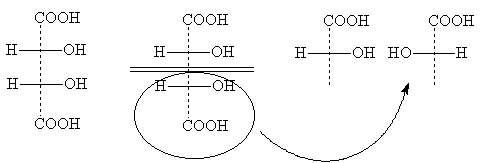
Формулы II и III изображают оптические антиподы винной кислоты; при их смешении образуется оптически неактивный рацемат - виноградная кислота.
 2015-04-23
2015-04-23 1543
1543








