Кинетика ферментативной реакции (т. е. зависимость скорости реакции от ее условий) определяется в первую очередь свойствами катализатора, вследствие чего она значительно сложнее, чем кинетика некаталитических реакций.
Простейшим описанием кинетики (англ. Enzyme kinetics) односубстратных ферментативных реакций является уравнение Михаэлиса — Ментен.
Уравне́ние Михаэ́лиса — Ме́нтен — основное уравнение ферментативной кинетики, описывает зависимость скорости реакции, катализируемой ферментом, от концентрации субстрата и фермента. Простейшая кинетическая схема, для которой справедливо уравнение Михаэлиса:
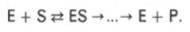
Уравнение имеет вид:
Где
V — максимальная скорость реакции, равная;
Km — константа Михаэлиса, равная концентрации субстрата, при которой скорость реакции составляет половину от максимальной;
 2015-04-30
2015-04-30 598
598








