| Щёлочи | Нерастворимые основания |
| 1. Действие на индикаторы. | |
| лакмус - синий фенолфталеин - малиновый | –– |
| 2. Взаимодействие с кислотными оксидами. | |
| 2KOH + CO2 ® K2CO3 + H2O KOH + CO2 ® KHCO3 | –– |
| 3. Взаимодействие с кислотами (реакция нейтрализации) | |
| NaOH + HNO3 ® NaNO3 + H2O | Cu(OH)2 + 2HCl ® CuCl2 + 2H2O |
| 4. Обменная реакция с солями | |
| Ba(OH)2 + K2SO4 ® 2KOH + BaSO4¯ 3KOH+Fe(NO3)3 ® Fe(OH)3¯ + 3KNO3 | –– |
| 5. Термический распад. | |
| –– | Cu(OH)2 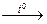 CuO + H2O CuO + H2O
|
| 6. Амфотерные основания взаимодействуют | |
| – с кислотами, проявляя свойства оснований: Zn(OH)2 + H2SO4 ® ZnSO4 + 2H2O – с основаниями, проявляя свойства кислот: Zn(OH)2 + 2NaOH ® Na2ZnO2 +2 H2O (при сплавлении) Zn(OH) 2 + 2NaOH ® Na2[Zn(OH)4] (в растворе) |
КИСЛОТЫ
Кислоты - сложные вещества, состоящие из атомов водорода и кислотного остатка. (С точки зрения теории электролитической диссоциации: кислоты - электролиты, которые при диссоциации в качестве катионов образуют только ионы водорода H+ и анионы кислотного остатка).
 2015-05-18
2015-05-18 282
282








