Методы экспериментального определения Кд основаны на особых способах графического отображения результатов измерения электропроводности.
В растворах слабых электролитов концентрация ионов невелика, расстояния между ними значительны, поэтому можно считать, что электростатические взаимодействия отсутствуют, ионы способны передвигаться с большой скоростью.
Степень диссоциации слабого электролита отражает долю молекул, распавшихся на ионы и равна отношению молярной электропроводности раствора к электроповодности при бесконечном разбавлении 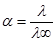 . Согласно закону разбавления Оствальда Кд = Сa2/(1 − a). Для разбавленных растворов
. Согласно закону разбавления Оствальда Кд = Сa2/(1 − a). Для разбавленных растворов 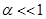 и Кд =Сa2. Тогда
и Кд =Сa2. Тогда
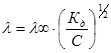
что объясняет нелинейность зависимости слабого электролита от С1/2 (в отличие от сильных электролитов).
Логарифмирование приводит к уравнению прямой в координатах lgl — lgC:
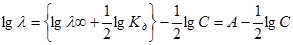
Линейная зависимость lgl от lgС наблюдается экспериментально при условии, что 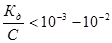 .
.
Кд вычисляют из найденной графически величины А (рис.9)
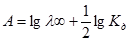 .
.

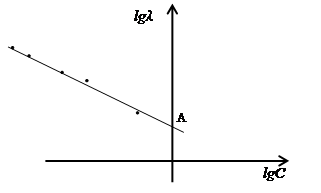
Рис. 9. Определение Кд слабого электролита по уравнению 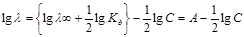
 2015-05-10
2015-05-10 271
271








