Путь ассимиляции аммиака, катализируемый системой глу-таминсинтетаза —Глутаматсинтаза, считается основным путем связывания NH3, образующегося в хлоропласте в результате редукции нитратов. Оба пути первичной ассимиляции NH3 с участием ГДГ или ГС — ГТС, как можно видеть из приведенных уравнений реакций, в конечном счете ведут к накоплению глутамата. Полагают, что ГДГ более активна у растений в темноте и в условиях аммонийного питания, тогда как ГС— ГТС —на свету и при питании нитратами.
Помимо а-кетоглутаровой кислоты, играющей основную роль в первичном связывании аммиака, роль акцепторов аммиака в, растениях могут выполнять и другие органические кето- и альдегидокислоты, которые с помощью соответствующих ферментов взаимодействуют с NH3 с образованием так называемых первичных аминокислот. Они же служат акцептором аминных групп в различных реакциях
 переаминирования. К числу этих органических кислот относятся щавелевоуксусная, пировиноградная, гидроксипи-ровиноградная, глиоксиловая и ряд других, в процессе восстановительного аминирования которых получаются соответственно аспарагиновая кислота, аланин, серии, глицин.
переаминирования. К числу этих органических кислот относятся щавелевоуксусная, пировиноградная, гидроксипи-ровиноградная, глиоксиловая и ряд других, в процессе восстановительного аминирования которых получаются соответственно аспарагиновая кислота, аланин, серии, глицин.
Аминная группа глутамата может быть перенесена на другие кетокислоты в процессе трансаминирования, который был открыт в 1937 г. советскими биохимиками А. Е. Браунштейном и М. Г. Крицман. Энзимы, катализирующие эту реакцию, получили название аминотрансфераз. В качестве примера рассмотрим перенос NH2-группы глутамата на пировиноградную кислоту с образованием аланина:


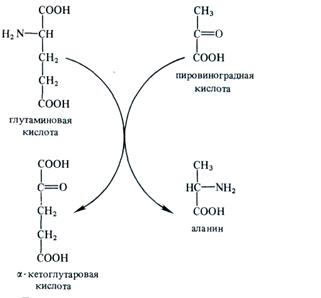
Трансаминирование с использованием аминогруппы глутамата широко распространено в растениях, обеспечивая возможность синтеза ряда аминокислот. Наиболее важные акцепторы NН2-группы в процессе трансаминирования и соответствующие им аминокислоты приведены ниже:
Акцепторы NН2-группы Аминокислоты
α-Кетоглутаровая Глутаминовая
Щавелевоуксусная Аспарагиновая
Глиоксиловая Глицин
Пировиноградная Аланин
Гидроксипировиноградная Серии
Фенилпировиноградная Фенилаланин
 При обильном снабжении растений аммонийными источниками азота в их тканях в значительном количестве накапливаются амиды — глутамин и аспарагин. Это явление было обнаружено и изучалось в классических работах Э. Шульце, Д. Н. Прянишникова, А. Чибнелла, а в последние 30 лет - В. Л. Кретовичем с сотрудниками. Особенно большой вклад в изучение роли амидов в растениях внес Прянишников, который рассматривал эти соединения как обезвреживающую, запасающую и транспортную форму азота в растениях. Исследования Кретовича с сотрудниками показали, что 15N включается в амидные группы амидов в 2 — 3 раза интенсивнее, чем в аминные. В то же время у большинства растений глутамин преобладает над аспарагином.
При обильном снабжении растений аммонийными источниками азота в их тканях в значительном количестве накапливаются амиды — глутамин и аспарагин. Это явление было обнаружено и изучалось в классических работах Э. Шульце, Д. Н. Прянишникова, А. Чибнелла, а в последние 30 лет - В. Л. Кретовичем с сотрудниками. Особенно большой вклад в изучение роли амидов в растениях внес Прянишников, который рассматривал эти соединения как обезвреживающую, запасающую и транспортную форму азота в растениях. Исследования Кретовича с сотрудниками показали, что 15N включается в амидные группы амидов в 2 — 3 раза интенсивнее, чем в аминные. В то же время у большинства растений глутамин преобладает над аспарагином.
Синтез глутамина был рассмотрен в разделе 6.3.4. Синтез аспарагина у растений может происходить двумя путями:

 Обе реакции катализируются ферментом аспарагинсинтетазой. Первая реакция прямого синтеза аспарагина из аспарагиновой кислоты и NH3 аналогична синтезу глутамина, катализируемому глутаминсинтетазой. Во второй реакции аспа-рагин образуется в результате переаминирования глутамина и аспарагиновой кислоты. Механизмы этих реакций пока мало исследованы. Аспарагинсинтетаза локализована в цитоплазме. Второй путь синтеза аспарагина, при котором донором NH2-группы служит глутамин, по-видимому, значительно более распространен в растениях, так как сродство фермента ас-парагинсинтетазы к глутамину в 10 раз выше, чем к иону NH4+. Аспарагиновая кислота возникает в результате переаминирования с участием щавелевоуксусной кислоты. Прямой синтез аспарагина в соответствии с первой реакцией может осуществляться в условиях избыточно высокого уровня NH+4 в тканях.
Обе реакции катализируются ферментом аспарагинсинтетазой. Первая реакция прямого синтеза аспарагина из аспарагиновой кислоты и NH3 аналогична синтезу глутамина, катализируемому глутаминсинтетазой. Во второй реакции аспа-рагин образуется в результате переаминирования глутамина и аспарагиновой кислоты. Механизмы этих реакций пока мало исследованы. Аспарагинсинтетаза локализована в цитоплазме. Второй путь синтеза аспарагина, при котором донором NH2-группы служит глутамин, по-видимому, значительно более распространен в растениях, так как сродство фермента ас-парагинсинтетазы к глутамину в 10 раз выше, чем к иону NH4+. Аспарагиновая кислота возникает в результате переаминирования с участием щавелевоуксусной кислоты. Прямой синтез аспарагина в соответствии с первой реакцией может осуществляться в условиях избыточно высокого уровня NH+4 в тканях.
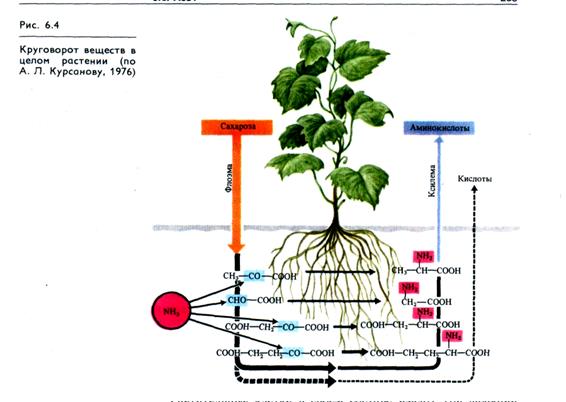
При выращивании растений на аммонийных источниках азота связывание NH+4 в виде амидов происходит уже в корнях. В этом случае более половины азота, транспортируемого из корней с пасокой, находится в форме амидов. Участие корней в связывании поглощенного аммония подтверждает представление Д. А. Сабинина, развитое в дальнейшем акад. А. Л. Курсановым, об активной роли корневой системы в синтезе органических соединений (рис. 6.4.). В корнях в результате процессов аминирования, амидирования и переаминирования могут синтезироваться более 25 видов азотных соединений. Роль углеродных скелетов в этих реакциях играют органические кислоты - продукты гликолиза и цикла Кребса. Практически весь азот, поглощенный в форме NH/, ассимилируется в корневой системе и поступает в надземные части в виде аминокислот и амидов.
В условиях нитратного питания ассимиляция NO-3 у растений осуществляется и в листьях. В этом случае акцепторами выступают первичные продукты фотосинтеза и фотодыхания. Поэтому набор аминокислот, синтезируемых в листьях, может быть качественно иным: больше синтезируется сложных и ароматических аминокислот.
Растительные клетки в своем составе имеют три фракции веществ, содержащих азот,— неорганический азот, низкомолекулярные и высокомолекулярные органические формы азота, находящиеся в определенном равновесии между собой:
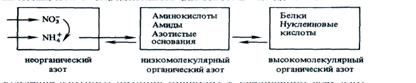
Усиление азотного питания приводит к увеличению всех азотсодержащих фракций. При этом особенно сильно возрастает количество растворимых аминосоединений, тогда как содержание белка повышается только до определенной величины.
В зеленых растениях белковый азот — основная азотсодержащая фракция, составляющая 80 — 95%, доля азота нуклеиновых кислот - около 10%, аминокислот и амидов - 5 % от суммарного азота, присутствующего в растительном материале. В вегетативных частях растений белки представлены главным образом ферментами, тогда как в семенах основная часть белковой фракции приходится на запасные белки. Азот входит также в состав фосфолипидов, коэнзимов, хлорофилла, фитогормонов (ауксина, цитокинина) и других соединений.
 Фосфор, как и азот, — важнейший элемент питания растений. Он поглощается ими в виде высшего окисла РО3-4 и не изменяется, включаясь в органические соединения. В растительных тканях концентрация фосфора составляет 0,2—1,3% от сухой массы растения.
Фосфор, как и азот, — важнейший элемент питания растений. Он поглощается ими в виде высшего окисла РО3-4 и не изменяется, включаясь в органические соединения. В растительных тканях концентрация фосфора составляет 0,2—1,3% от сухой массы растения.
Запасы фосфора в пахотном слое почвы относительно невелики, порядка 2,3 — 4,4 т/га (в пересчете на P2О5). Из этого количества 2/з приходится на минеральные соли ортофосфор-ной кислоты (Н3РО4), а 1/3 ~на органические соединения, содержащие фосфор (органические остатки, гумус, фитат и др.). Фитаты составляют до половины органического фосфора почвы. Большая часть фосфорных соединений слабо растворима в почвенном растворе. Это, с одной стороны, снижает потери фосфора из почвы за счет вымывания, но, с другой, — ограничивает возможности использования его растениями.
Основной природный источник поступления фосфора в пахотный слой — выветривание почвообразующей породы, где он содержится главным образом в виде апатитов ЗСа3(РО4)2 • CaF2 и др. Трехзамещенные фосфорные соли кальция и магния и соли полуторных оксидов железа и алюминия (FePO4, A1PO4 в кислых почвах) слаборастворимы и малодоступны для растений. Двузамещенные и особенно однозамещенные соли кальция и магния, тем более соли одновалентных катионов и свободная ортофосфорная кислота растворимы в воде и используются растениями как главный источник фосфора в почвенном растворе. Растения способны усваивать и некоторые органические формы фосфора (фосфаты Сахаров, фитин). Концентрация фосфора в почвенном растворе невелика (0,1 — 1 мг/л).
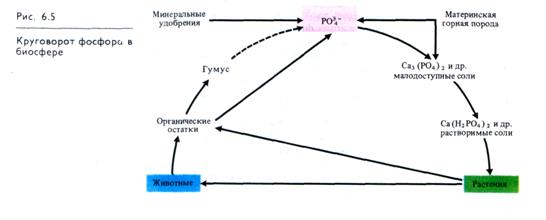
Схема круговорота фосфора в биосфере представлена на рис. 6.5. Фосфор органических остатков и гумуса минера-лизуется почвенными микроорганизмами и большая его часть превращается в малорастворимые соли. Растения получают из них фосфор, делая его более подвижным. Это достигается благодаря выделению корнями органических кислот, которые хелатируют двухвалентные катионы и подкисляют ризосферу, способствуя переходу НРО3-4 →НРО2-4|→ НРО-4. Некоторые сельскохозяйственные культуры хорошо усваивают труднорастворимые фосфаты (люпин, гречиха, горох). Эта способность у растений увеличивается с возрастом.

В растительных тканях фосфор присутствует в органической форме и в виде ортофосфорной кислоты и ее солей. Он входит в состав белков (фосфопротеинов), нуклеиновых кислот, фосфолипидов, фосфорных эфиров Сахаров, нуклеотидов, принимающих участие в энергетическом обмене (АТР, NAD+ и др.), витаминов и многих других соединений.
Фосфор играет особо важную роль в энергетике клетки, поскольку именно в форме высокоэнергетических эфирных связей фосфора (С—О ~ Р) или пирофосфатных связей в нуклеозидди-, нуклеозидтрифосфатах и в полифосфатах запасается энергия в живой клетке. Эти связи обладают высокой стандартной свободной энергией гидролиза (например, 14 кДж/моль у глюкозо-6-фосфата и AMP, 30,5 — у ADP и АТР и 62 кДж/моль — у фосфоенолпирувата). Это настолько универсальный способ запасания и использования энергии, что почти во всех метаболических путях участвуют те или иные фосфорные эфиры и (или) нуклеотиды, а состояние адениннуклеотидной системы (энергетический заряд) - важный механизм контроля дыхания (см. 4.4.3).
В форме стабильного диэфира фосфат входит составной частью в структуру нуклеиновых кислот и фосфолипидов. В нуклеиновых кислотах фосфор образует мостики между нуклеозидами, объединяя их в гигантскую цепочку. Фосфат обусловливает гидрофильность фосфолипида, тогда как остальная часть молекулы липофильна. Поэтому на границе раздела фаз в мембранах молекулы фосфолипидов ориентируются полярно, фосфатными концами наружу, а липофильное ядро молекулы прочно удерживается в липидном бислое, стабилизируя мембрану.
Еще одной уникальной функцией фосфора является его участие в фосфорилировании клеточных белков с помощью протеинкиназ. Этот механизм контролирует многие процессы метаболизма, так как включение фосфата в молекулу белка приводит к перераспределению в ней электрических зарядов и вследствие этого к модификации ее структуры и функции. Фосфорилирование белков регулирует такие процессы, как синтез РНК и белка, деление, дифференцировка клеток и многие другие.
Основной запасной формой фосфора у растений является фитин ~ кальций- магниевая соль инозитфосфорной кислоты (инозитолгексафосфата):
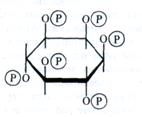
Значительные количества фитина (0,5 — 2% на сухую массу) накапливаются в семенах, составляя до 50% от общего фосфора в них.
Радиальное передвижение фосфора в зоне поглощения корня до ксилемы происходит по симпласту, причем его концентрация в клетках корня в десятки — сотни раз превышает концентрацию фосфата в почвенном растворе. Транспорт по ксилеме осуществляется в основном или полностью в форме неорганического фосфата; в этом виде он достигает листьев и зон роста. Фосфор, как и азот, легко перераспределяется между органами. Из клеток листьев он поступает в ситовидные трубки и по флоэме транспортируется в другие части растения, особенно в конусы нарастания и в развивающиеся плоды. Аналогичный отток фосфора происходит и из стареющих листьев.
Внешним симптомом фосфорного голодания является синевато-зеленая окраска листьев нередко с пурпурным или бронзовым оттенком (свидетельство задержки синтеза белка и накопления Сахаров). Листья становятся мелкими и более узкими. Приостанавливается рост растений, задерживается созревание урожая.
При дефиците фосфора снижается скорость поглощения кислорода, изменяется активность ферментов, участвующих в дыхательном метаболизме, начинают активнее работать некоторые немитохондриальные системы окисления (оксидаза гликолевой кислоты, аскорбатоксидаза). В условиях фосфорного голодания активируются процессы распада фосфорорганических соединений и полисахаридов, тормозится синтез белков и свободных нуклеотидов.
Наиболее чувствительны к недостатку фосфора растения на ранних этапах роста и развития. Нормальное фосфорное питание в более поздний период ускоряет развитие растений (в противоположность азотному), что в южных районах позволяет уменьшить вероятность их попадания под засуху, а в северных — под заморозки.
 Сера входит в число основных питательных элементов, необходимых для жизни растения. Она поступает в них главным образом в виде сульфата. Ее содержание в растительных тканях относительно невелико и составляет 0,2—1,0% в расчете на сухую массу. Потребность в сере высока у растений, богатых белками, например у бобовых (люцерна, клевер), но особенно сильно она выражена у представителей семейства крестоцветных, которые в больших количествах синтезируют серосодержащие горчичные масла.
Сера входит в число основных питательных элементов, необходимых для жизни растения. Она поступает в них главным образом в виде сульфата. Ее содержание в растительных тканях относительно невелико и составляет 0,2—1,0% в расчете на сухую массу. Потребность в сере высока у растений, богатых белками, например у бобовых (люцерна, клевер), но особенно сильно она выражена у представителей семейства крестоцветных, которые в больших количествах синтезируют серосодержащие горчичные масла.
 Сера, как и все биогенные элементы, участвует в биологическом круговороте веществ. Автотрофные растения поглощают серу в виде высшего окисла SO4, восстанавливая его до уровня SH-rpyпп органических веществ. Органическая сера в виде растительных и животных остатков попадает в почву и водоемы и минерализуется сапрофитными микроорганизмами до H2S, причем часть сероводорода может превращаться в нерастворимые соединения (FeS), а часть освобождаться в атмосферу. Бесцветные серобактерии-хемосинтетики в присутствии кислорода и пурпурные и зеленые серобактерии-фотосинтетики в анаэробных условиях (см. 3.1.2) окисляют сероводород до свободной серы и сульфата: H2S→ S° → SО2-з→ SO2-4. Наоборот, сульфатвосстанавливающие бактерии-хемосинтетики в условиях анаэробиоза используют сульфат как источник кислорода: 4Н2 + SO2-4→ S2- + 4Н2О (сульфатное дыхание). Все эти превращения можно представить в виде следующей схемы:
Сера, как и все биогенные элементы, участвует в биологическом круговороте веществ. Автотрофные растения поглощают серу в виде высшего окисла SO4, восстанавливая его до уровня SH-rpyпп органических веществ. Органическая сера в виде растительных и животных остатков попадает в почву и водоемы и минерализуется сапрофитными микроорганизмами до H2S, причем часть сероводорода может превращаться в нерастворимые соединения (FeS), а часть освобождаться в атмосферу. Бесцветные серобактерии-хемосинтетики в присутствии кислорода и пурпурные и зеленые серобактерии-фотосинтетики в анаэробных условиях (см. 3.1.2) окисляют сероводород до свободной серы и сульфата: H2S→ S° → SО2-з→ SO2-4. Наоборот, сульфатвосстанавливающие бактерии-хемосинтетики в условиях анаэробиоза используют сульфат как источник кислорода: 4Н2 + SO2-4→ S2- + 4Н2О (сульфатное дыхание). Все эти превращения можно представить в виде следующей схемы:
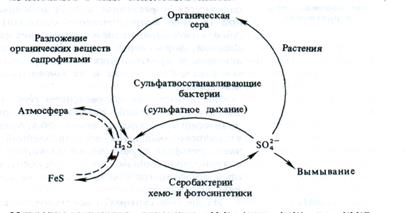
Микробиологическое окисление H2S (или FeS) до SO2-4| сопровождается подкислением почвы. Сульфат относительно лабилен в почвах и частично вымывается.
В почве сера находится в неорганической и органической формах. В большинстве почв преобладает органическая сера растительных и животных остатков, а в торфянистых почвах она может составлять до 100% всей серы. Основная неорганическая форма серы в почве — сульфат, который может находиться в виде солей CaSO4, MgSO4, Na2SO4 в почвенном растворе в ионной форме или адсорбированным на почвенных коллоидах. В засоленных Na2SO4 почвах содержание сульфата может достигать 60% от массы почвы. В затопляемых почвах сера находится в восстановленной форме в виде FeS, РеS2 или H2S. Суммарное содержание серы в почвах умеренных климатических зон составляет в среднем 0,005 — 0,040%.
 Растения поглощают серу главным образом в форме сульфата. Трансмембранный перенос сульфата осуществляется в котранспорте с Н+ или в обмен на ионы HCO-3. Менее окисленные (SO2) или более восстановленные (H3S) неорганические соединения серы токсичны для растений. Очень слабо воспринимают растения и органические соединения (аминокислоты), содержащие восстановленную серу.
Растения поглощают серу главным образом в форме сульфата. Трансмембранный перенос сульфата осуществляется в котранспорте с Н+ или в обмен на ионы HCO-3. Менее окисленные (SO2) или более восстановленные (H3S) неорганические соединения серы токсичны для растений. Очень слабо воспринимают растения и органические соединения (аминокислоты), содержащие восстановленную серу.
 В последнее время появились данные о том, что растения в качестве источника серы способны использовать SO2 атмосферы. Благоприятный эффект низких концентраций SO2 в воздухе на рост наблюдался при выращивании растений в
В последнее время появились данные о том, что растения в качестве источника серы способны использовать SO2 атмосферы. Благоприятный эффект низких концентраций SO2 в воздухе на рост наблюдался при выращивании растений в
 отсутствие SO2-4 в питательной среде. Однако подобное действие диоксид серы может оказывать лишь в концентрации порядка 0,1-0,2 мг серы SО2/м3. При содержании SO2 в атмосфере свыше 0,5 — 0,7 мг серы SО2/м3 диоксид серы становится токсичным, вызывая некрозы листьев, что объясняется накоплением в тканях SO2, анионов HSO-3 и SO2-3. Эти соединения разобщают фотофосфорилирование, а также разрушают мембраны хлоропластов.
отсутствие SO2-4 в питательной среде. Однако подобное действие диоксид серы может оказывать лишь в концентрации порядка 0,1-0,2 мг серы SО2/м3. При содержании SO2 в атмосфере свыше 0,5 — 0,7 мг серы SО2/м3 диоксид серы становится токсичным, вызывая некрозы листьев, что объясняется накоплением в тканях SO2, анионов HSO-3 и SO2-3. Эти соединения разобщают фотофосфорилирование, а также разрушают мембраны хлоропластов.
Содержание, формы и транспорт серы в растениях. Сера содержится в растениях в двух основных формах — окисленной (в виде неорганического сульфата) и восстановленной. Абсолютное содержание и соотношение окисленной и восстановленной форм серы в органах растений зависит как от активности протекающих в них процессов редукции и ассимиляции сульфата, так и от концентрации SО4 в питательной среде.
Часть поглощенной растением серы задерживается в сульфатном пуле корней, возможно, в форме CaSO4 или метаболического сульфата, вновь образующегося в результате вторичного окисления восстановленной серы. Основная же часть сульфата перемещается из корней в сосуды ксилемы и с транспирационным током переносится к молодым растущим органам, где она интенсивно включается в обмен и теряет подвижность.
Из листьев сульфат и восстановленные формы серы (серо- содержащие аминокислоты, глутатион) могут перемещаться по флоэме как акропетально, так и базипетально в растущие части растений и в запасающие органы. В семенах сера находится преимущественно в органической форме, а в процессе их прорастания частично переходит в окисленную. Редукция сульфата и синтвв серосодержащих аминокислот и белков наблюдается при созревании семян.
Доля сульфата в общем балансе серы в тканях может колебаться от 10 до 50% и более. Она минимальна в молодых листьях и резко возрастает при их старении в связи с усилением процессов деградации серосодержащих белков.
Механизмы восстановления и ассимиляции серы. В большинстве серосодержащих органических соединений сера находится в восстановленной форме. Это означает, что сульфат, поступивший в растение, подвергается восстановлению. У высших растений весьма развита сульфатредуцирующая способность. Процесс восстановления сульфата, обеспечивающий включение серы в серосодержащие аминокислоты, локализован преимущественно в листьях (в хлоропластах) и является ключевым в ассимиляции серы высшими растениями. Включение серы в органические вещества изучалось в основном на грибах, но исследования последних лет показали, что у высших растений этот процесс осуществляется принципиально так же (Н. И. Шевякова, 1979). При этом происходит активирование сульфата, восстановление серы и, наконец, ее включение в органические соединения.
Активация сульфата осуществляется при участии АТР, благодаря которому относительно инертный оксид серы вступает в метаболический цикл. Этот процесс у большинства растений протекает в соответствии с уравнением:
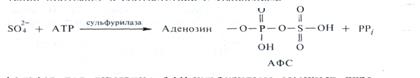
Сульфат под действием АТР-сульфурилазы замещает пиро-фосфорильную группу в АТР, в результате чего образуются аденозин-5-фосфосульфат (АФС) и пирофосфат (РРi). Активность АТР-сульфурилазы контролируется эндогенным уровнем сульфата путем репрессии и дерепрессии синтеза фермента, а также концентрацией в клетке серосодержащих аминокислот. Активированный в форме АФС сульфат затем подвергается восстановлению, сопряженному с переносом восьми электронов. Общая затрата энергии в этом процессе составляет 496 кДж, что несколько меньше энергии, потребляемой на восстановление NO3- до NH4-. Установлено, что восстановление SO2-4 осуществляете АФС-редуктазным комплексом, состоящим из двух ферментов (АФС-сульфотрансферазы и тиосульфонатре-дуктазы), низкомолекулярного SH-белка — акцептора сульфо- группы (SH — носителя) и кофактора (ферредоксина). Последовательность реакций при участии АФС-редуктазного комплекса можно представить следующим образом:

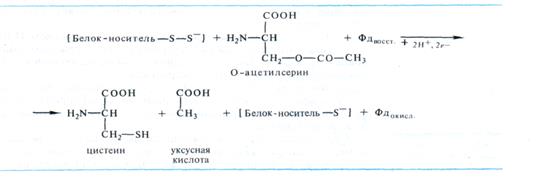
Предполагается, что белок, акцептирующий сульфогруппу, является простетической группой тиосульфонатредуктазы. Восстановление сульфогруппы до тиоловой при помощи ферредоксина происходит прямо на белке-носителе. На последнем этапе тиоловая группа от белка-носителя передается на О- ацетилсерин (механизм неизвестен), и в результате регенерирует исходная форма носителя, а из ацетилсерина образуются цистеин и ацетат:
ментов, играя важную роль во взаимодействии белка с ко-ферментом.
Многие виды растений в малых количествах содержат летучие соединения серы. Например, сульфоксиды R—S—R входят в состав фитонцидов лука и чеснока. Именно их присутствие вызывает раздражение глаз при нарезании лука. Недостаточное снабжение растений серой тормозит синтез серосодержащих аминокислот и белков, снижает фотосинтез и скорость роста растений, особенно надземной части. В острых случаях нарушается формирование хлоропластгв и возможен их распад. Симптомы дефицита серы-побледнение и пожелтение листьев — похожи на признаки недостатка азота, но сначала появляются у самых молодых листьев. Это показывает, что отток серы из более старых листьев не может компенсировать недостаточное снабжение растений серой через корни.
 Калий — один из самых необходимых элементов минерального питания растений. Его содержание в тканях составляет в среднем 0,5-1,2% в расчете на сухую массу. Долгое время основным источников получения калия служила зола, что нашло отражение в названии элемента (potassium происходит от слова potashes — тигельная зола). Содержание калия в клетке в 100—1000 раз превышает его уровень во внешней среде. Его гораздо больше в тканях, чем других катионов.
Калий — один из самых необходимых элементов минерального питания растений. Его содержание в тканях составляет в среднем 0,5-1,2% в расчете на сухую массу. Долгое время основным источников получения калия служила зола, что нашло отражение в названии элемента (potassium происходит от слова potashes — тигельная зола). Содержание калия в клетке в 100—1000 раз превышает его уровень во внешней среде. Его гораздо больше в тканях, чем других катионов.
Запасы калия в почве больше содержания фосфора в 8-40 раз, а азота - в 5-50 раз. В почве калий может находиться в следующих формах: в составе кристаллической решетки минералов, в обменном и необменном состоянии в коллоидных частицах, в составе пожнивных остатков и микроорганизмах, в виде минеральных солей почвенного раствора.
Наилучшим источником питания являются растворимые соли калия (0,5 — 2% от валовых запасов в почве). По мере потребления подвижных форм калия запасы его в почве могут восполняться за счет обменных форм, а при уменьшении последних — за счет необменных, фиксированных форм калия. Попеременное подсушивание и увлажнение почвы, а также деятельность корневой системы растений и микроорганизмов способствуют переходу калия в доступные формы.
 Калийные удобрения хорошо растворимы в воде. При попадании в почву калий вступает в обменное взаимодействие с коллоидами почвы. В результате 25 — 80% калия может связываться почвенным поглощающим комплексом. При этом в почвенный раствор вытесняются ионы водорода, кальций, алюминий, магний, марганец и другие катионы. По своему характеру калийные удобрения - физиологически кислые соли, способствующие накоплению в почве хлорной и серной кислот. Поэтому на кислых почвах эффективность калийных удобрений без известкования снижается.
Калийные удобрения хорошо растворимы в воде. При попадании в почву калий вступает в обменное взаимодействие с коллоидами почвы. В результате 25 — 80% калия может связываться почвенным поглощающим комплексом. При этом в почвенный раствор вытесняются ионы водорода, кальций, алюминий, магний, марганец и другие катионы. По своему характеру калийные удобрения - физиологически кислые соли, способствующие накоплению в почве хлорной и серной кислот. Поэтому на кислых почвах эффективность калийных удобрений без известкования снижается.
В растениях калий в наибольшем количестве сосредоточен в молодых, растущих тканях, характеризующихся высоким уровнем обмена веществ: меристемах, камбии, молодых листьях, побегах, почках. В клетках калий присутствует в основном в ионной форме, он не входит в состав органических соединений, имеет высокую подвижность и поэтому легко реутилизируется. Передвижению калия из старых в молодые листья способствует натрий, который может замещать его в тканях растений, прекративших рост.
В растительных клетках около 80% калия содержится в вакуолях. Он составляет основную часть катионов клеточного сока. Поэтому калий может вымываться из растений дождями, особенно из старых листьев. Небольшая часть этого катиона (около 1 %) прочно связана с белками митохондрий и хлоропластов. Калий стабилизирует структуру этих органелл. При калиевом голодании нарушается ламеллярно-гранулярное строение хлоропластов и дезорганизуются мембранные структуры митохондрий. До 20% калия клетки адсорбируется на коллоидах цитоплазмы. На свету прочность связи калия с коллоидами выше, чем в темноте. В ночное время может наблюдаться даже выделение калия через корневую систему растений.
Калий служит основным иротивоионом для нейтрализации отрицательных зарядов неорганических и органических' анионов. Именно присутствие калия в значительной степени определяет коллоидно-химические свойства цитоплазмы, что существенно влияет практически на все процессы в клетке. Калий способствует поддержанию состояния гидратации коллоидов цитоплазмы, регулируя ее водоудерживающую способность. Увеличение гидратации белков и водоудерживающей способности цитоплазмы повышает устойчивость растений к засухе и морозам.
Калий необходим для поглощения и транспорта воды по растению. Расчеты показывают, что работа «нижнего концевого двигателя», т. е. корневого давления, на 3/4 обусловлена присутствием в пасоке ионов калия. Важное значение калий имеет в процессе открывания и закрывания устьиц. На свету в вакуолях замыкающих клеток устьиц концентрация ионов калия резко возрастает (в 4 — 5 раз), что приводит к быстрому входу воды, повышению тургора и открыванию устьичной щели. В темноте калий начинает выходить из замыкающих клеток, тургорное давление в них падает и устьица закрываются.
Калий поглощается растениями в виде катиона и образует лишь слабые связи с различными соединениями в клетке. Вероятно, поэтому именно калий создает ионную асимметрию и разность электрических потенциалов между клеткой и средой (мембранный потенциал).
Калий является одним из катионов — активаторов ферментативных систем. В настоящее время известно более 60 ферментов, активируемых калием с различной степенью специфичности. Он необходим для включения фосфата в органические соединения, реакций переноса фосфатных групп, для синтеза белков и гюлисахаридов и участвует в синтезе рибофлавина — компонента всех флавиновых дегидрогеназ. Под влиянием калия увеличивается накопление крахмала в клубнях картофеля, сахарозы в сахарной свекле, моносахаридов в плодах и овощах, целлюлозы, гемицеллюлоз и пектиновых веществ в клеточной стенке растений. В результате повышается устойчивость соломины злаков к полеганию, у льна и конопли улучшается качество волокна. Достаточное снабжение растений калием повышает их устойчивость к грибковым и бактериальным заболеваниям.
 Некоторые одновалентные катионы со сходными физико-химическими свойствами в ряде случаев могут заменить калий в процессах, где требуется его участие. По своим свойствам наиболее близки к калию NH+4 и Rb+. Ион аммония способен заменять калий в активации ферментов на 50—100%, рубидий-на 20-80, Na+, Li+ и Cs+- на 5-20% или они вообще не активны. Однако накопление аммония в растениях может вызывать токсический эффект, а содержание ионов рубидия в клетках обычно невелико.
Некоторые одновалентные катионы со сходными физико-химическими свойствами в ряде случаев могут заменить калий в процессах, где требуется его участие. По своим свойствам наиболее близки к калию NH+4 и Rb+. Ион аммония способен заменять калий в активации ферментов на 50—100%, рубидий-на 20-80, Na+, Li+ и Cs+- на 5-20% или они вообще не активны. Однако накопление аммония в растениях может вызывать токсический эффект, а содержание ионов рубидия в клетках обычно невелико.
В отсутствие калия основным катионом, способным заменить его, является натрий. Иногда 2/3 необходимого растениям калия может быть без видимых нарушений заменено натрием. Степень такой заместимости различна и зависит от вида растения. Однако многие ферменты, для которых необходим К+, активируются натрием незначительно или даже угнетаются. Высокие концентрации ионов натрия могут нарушать структуру хлоропластов и оказывать вредное воздействие на некоторые процессы обмена веществ. Положительное влияние натрия на развитие растений проявляется при недостатке калия. Если же калия в среде достаточно, избыток натрия может быть токсичном.
Следует отметить, что при снижении уровня калия в клетке увеличивается содержание натрия, магния, кальция, свободного аммиака, ионов водорода, минеральных фосфатов. Калий способствует усвоению растениями иона аммония. При аммиачном питании резко возрастает потребность в снабжении калием, особенно у злаков. При недостатке калия аммиачное питание приводит к излишнему накоплению NH+4 и отравлению растений.
Критический период в снабжении калием приходится на ранние стадии роста растений (первые две недели после всходов). Наибольшее же его количество поглощается, как правило, в период интенсивного нарастания вегетативной массы. У зерновых и зернобобовых поступление калия заканчивается к началу молочной спелости, у льна — в фазу цветения, у картофеля, сахарной свеклы, капусты максимум поглощения калия приходится на период формирования клубней, корнеплодов, кочанов. Особенно высока концентрация калия в овощных культурах — огурцах, томатах, капусте. Однако потребление калия подсолнечником превосходит все остальные культуры. Так, при уборке вместе с урожаем выносится калия (К2О):
 2015-05-26
2015-05-26 2840
2840
