картофелем и злаками — 180 кг/га, капустой — 280, семенами подсолнечника — 990 кг/га.
При недостатке калия начинается пожелтение листьев снизу вверх — от старых к молодым. Листья желтеют с краев. В дальнейшем их края и верхушки приобретают бурую окраску, иногда с красными «ржавыми» пятнами; происходит отмирание и разрушение этих участков. Листья выглядят как бы обожженными. Снабжение калием особенно важно для молодых, активно растущих органов и тканей. Поэтому при калиевом голодании снижается функционирование камбия, нарушается развитие сосудистых тканей, уменьшается толщина клеточной стенки эпидермиса и кутикулы, тормозятся процессы деления и растяжения клеток. В результате укорачивания междоузлий могут образоваться розеточные формы растений. Недостаток калия приводит к снижению доминирующего эффекта апикальных почек. Верхушечные и верхушечно-боковые почки перестают развиваться и отмирают, активируется рост боковых побегов и растение приобретает форму куста.
Недостаток калия снижает продуктивность фотосинтеза, прежде всего за счет уменьшения скорости оттока ассими-лятов из листьев: при калиевом голодании она падает более чем в два раза. В этом случае ни фосфорные, ни азотные удобрения не могут заменить калий. Двукратное повышение содержания калия в питательном растворе в 1,5 раза увеличивало скорость оттока меченных по 14С растворимых ассимилятов из листьев томатов, при этом в плодах содержание метки возрастало в 2 раза.
 Общее содержание кальция у разных видов растений составляет 5 —30 мг на 1 г сухой массы. Растения по отношению к кальцию делят на три группы: кальциефилы, кальциефобы и нейтральные виды. Много кальция содержат бобовые, гречиха, подсолнечник, картофель, капуста, конопля, гораздо меньше — зерновые, лен, сахарная свекла. В тканях двудольных растений этого элемента, как правило, больше, чем у однодольных.
Общее содержание кальция у разных видов растений составляет 5 —30 мг на 1 г сухой массы. Растения по отношению к кальцию делят на три группы: кальциефилы, кальциефобы и нейтральные виды. Много кальция содержат бобовые, гречиха, подсолнечник, картофель, капуста, конопля, гораздо меньше — зерновые, лен, сахарная свекла. В тканях двудольных растений этого элемента, как правило, больше, чем у однодольных.
Кальций накапливается в старых органах и тканях. Это связано с тем, что транспорт его осуществляется по ксилеме и реутилизация затруднена. При старении клеток или снижении их физиологической активности кальций из цитоплазмы перемещается в вакуоль и откладывается в виде нерастворимых солей щавелевой, лимонной и других кислот. Образующиеся кристаллические включения затрудняют подвижность и возможность повторного использования этого катиона.
 У большинства культурных растений кальций накапливается в вегетативных органах. В корневой системе содержание его ниже, чем в надземной части. В семенах кальций присутствует преимущественно как соль инозитфосфорной кислоты (фитин).
У большинства культурных растений кальций накапливается в вегетативных органах. В корневой системе содержание его ниже, чем в надземной части. В семенах кальций присутствует преимущественно как соль инозитфосфорной кислоты (фитин).
В клетке большое количество кальция связано с пектиновыми веществами срединной пластинки и клеточной стенки. Это — фонд обменного кальция. Он содержится также в хлоропластах, митохондриях и ядре в комплексах с биополимерами, в виде неорганических фосфатов и в ионизированной форме. В цитозоле (растворимой части цитоплазмы) концентрация Са2+ очень низка (10-7 – 10-6 моль/л).
Кальций выполняет многообразные функции в обмене веществ клеток и организма в целом. Они связаны с его влиянием на структуру мембран, ионные потоки через них и биоэлектрические явления, на перестройки цитоскелета, процессы поляризации клеток и тканей и др.
Локальные изменения концентрации Са2+ в цитоплазме играют важную роль в структурных перестройках компонентов цитоскелета — актиноподобных белков, участвующих в процессах движения цитоплазмы, обратимых изменениях ее вязкости (переходы гель — золь и обратно), в пространственной организации цитоплазматических ферментных систем (например, гликолиза). Процессы сборки — разборки микротрубочек также регулируются уровнем ионов Са2+ (наряду с Mg2+ и GTP). Кальций необходим для процессов секреции у растений, в частности для гранулокриновой секреции компонентов клеточных стенок с участием везикул АГ (см. рис. 10.8).
Кальций активирует ряд ферментных систем клетки: дегид-рогеназы (глутаматдегидрогеназа, малатдегидрогеназа, глю-козо-6-фосфатдегидрогеназа, NADP-зависимая изоцитратде-гидрогеназа), ос-амилазу, аденилат- и аргининкиназы, липазы, фосфатазы. При этом кальций может способствовать агрегации субъединиц белка, служить мостиком между ферментом и субстратом, влиять на состояние аллостерического центра фермента. Избыток кальция в ионной форме угнетает окислительное фосфорилирование и фотофосфорилирование.
Регулирующее влияние кальция на многие стороны метаболизма зависит от его взаимодействия с кальциевым внутриклеточным рецептором — белком кальмодулином. Название белка отражает его функцию модулятора Са-зависимых процессов. Это кислый (изоэлектрическая точка при рН 3,0 — 4,3), термостабильный низкомолекулярный (Мr= 16,7 кД, 148 аминокислот) белок. Обладает высоким сродством к кальцию, связывая четыре иона Са2+ на 1 моль. Комплекс Са2+ — кальмодулин активирует многие ферментные системы, например протеинкиназы, фосфодиэстеразу, транспортную Са2+-АТРазу, АТРазу динеина жгутиков, АТРазу актомиозина и др. С участием кальмодулина регулируется концентрация внутриклеточного кальция. Кальмодулин может связываться с различными мембранами в клетке и легко переходит в цитозоль, причем в присутствии Са2+ комплексы кальмодулина с другими белками более прочны, чем без Са2+. Комплекс Са2+ — кальмодулин в клетках активирует деятельность сократительных белков, тормозит разборку микротрубочек, участвует в секреторных и многих других процессах.
Влиянием Са2+ на сборку — разборку элементов цитоскелета объясняется его необходимость для процессов митоза. Концентрация кальция в комплексе с кальмодулином регулирует сборку микротрубочек веретена. Кальций участвует в слиянии везикул Гольджи при формировании фрагмопласта и новой клеточной стенки.
Для роста клеток растяжением также небезразличен уровень кальция в клетке. Ингибитор кальмодулина N-(6-аминогексил)-5-хлор-1-нафтилсульфонамидгидрохлорид подавляет удлинение колеоптилей овса и кукурузы, а его неактивные аналоги не влияют на рост растяжением. Повышенная концентрация кальция тормозит ауксинзависимый рост, но усиливает способность ИУК индуцировать электрофизиологическую поляризацию тканей. Кальций — необходимый компонент в механизме поляризации клеток.
Важная роль принадлежит ионам Са2+ в стабилизации мембран. Взаимодействуя с отрицательно заряженными группами фосфолипидов, он стабилизирует мембрану и снижает ее пассивную проницаемость. При недостатке кальция повышается проницаемость мембран, появляются их разрывы и фрагментация, нарушаются процессы мембранного транспорта.
Важно отметить, чтв почти вся катионообменная емкость поверхности корня занята кальцием и частично Н+. Это указывает на участие кальция в первичных механизмах поступления ионов в клетки корня. Ограничивая поступление других ионов в растения, кальций способствует устранению токсичности избыточных концентраций ионов аммония, алюминия, марганца, железа, повышает устойчивость растений к засолению, снижает кислотность почвы. Именно кальций чаще всего выступает в роли балансного иона при создании физиологической уравновешенности ионного состава среды, так как его содержание в почве достаточно велико.
От недостатка кальция в первую очередь страдают молодые меристематические ткани и корневая система. У делящихся клеток не образуются новые клеточные стенки и в результате возникают многоядерные клетки, характерные для меристем с дефицитом кальция. Прекращается образование боковых корней и корневых волосков, замедляется рост корней. Недостаток кальция приводит к набуханию пектиновых веществ, что вызывает ослизнение клеточных стенок и разрушение клеток. В результате корни, листья, отдельные участки стебля загнивают и отмирают. Кончики и края листьев вначале белеют, а затем чернеют, листовые пластинки искривляются и скручиваются. На плодах, в запасающих и сосудистых тканях появляются некротические участки. Нарушается структура плазмалеммы и мембран клеточных органелл.
 Большинство типов почв богато кальцием, и резко выраженное кальциевое голодание встречается редко, например при сильной кислотности или засоленности почв, на торфяниках, при нарушении развития корневой системы, при неблагоприятных погодных условиях.
Большинство типов почв богато кальцием, и резко выраженное кальциевое голодание встречается редко, например при сильной кислотности или засоленности почв, на торфяниках, при нарушении развития корневой системы, при неблагоприятных погодных условиях.
 По содержанию в растениях магний занимает четвертое место после калия, азота и кальция. У высших растений среднее его содержание в расчете на сухую массу 0,02 — 3,1%, у водорослей 3,0 — 3,5%. Особенно много его в растениях короткого дня — кукурузе, просе, сорго, конопле, а также в картофеле, свекле, табаке и бобовых. 1 кг свежих листьев содержит 300 — 800 мг магния, из них 30-80 мг (т. е. 1/10 часть) входит в состав хлорофилла. Особенно много магния в молодых клетках и растущих тканях, а также в генеративных органах и запасающих тканях. В зерновках магний накапливается в зародыше, где его уровень, в несколько раз превышает содержание в эндосперме и кожуре (для кукурузы соответственно 1,6, 0,04 и 0,19 % на сухую массу).
По содержанию в растениях магний занимает четвертое место после калия, азота и кальция. У высших растений среднее его содержание в расчете на сухую массу 0,02 — 3,1%, у водорослей 3,0 — 3,5%. Особенно много его в растениях короткого дня — кукурузе, просе, сорго, конопле, а также в картофеле, свекле, табаке и бобовых. 1 кг свежих листьев содержит 300 — 800 мг магния, из них 30-80 мг (т. е. 1/10 часть) входит в состав хлорофилла. Особенно много магния в молодых клетках и растущих тканях, а также в генеративных органах и запасающих тканях. В зерновках магний накапливается в зародыше, где его уровень, в несколько раз превышает содержание в эндосперме и кожуре (для кукурузы соответственно 1,6, 0,04 и 0,19 % на сухую массу).
Накоплению магния в молодых тканях способствует его сравнительно высокая подвижность в растениях, что обусловливает его вторичное использование (реутилизацию) из стареющих тканей. Однако степень реутилизации магния значительно ниже, чем азота, фосфора и калия. Легкая подвижность магния объясняется тем, что около 70% этого катиона в растении связано с анионами органических и неорганических кислот. Перемещение магния осуществляется как по ксилеме, так и по флоэме. Некоторая часть магния образует нерастворимые соединения, не способные к перемещению по растению (оксалат, пектат), другая его часть связывается высокомолекулярными соединениями. В семенах (зародыше, оболочке) большая часть магния находится в составе фитина. И, наконец, около 10—12% магния входит в состав хлорофилла. Эта последняя функция магния уникальна: ни один другой элемент не может заменить его в хлорофилле. Магний необходим для синтеза протопорфирина IX — непосредственного предшественника хлорофиллов.
На свету ионы магния освобождаются из полости тила-коидов в строму хлоропласта. Увеличение концентрации магния в строме активирует РДФ-карбоксилазу и другие ферменты. Предполагается, что возрастание концентрации Mg2+ (до 5 ммоль/л) в строме приводит к увеличению сродства РДФ-карбоксилазы к СО2 и активации восстановления СО2. Магний может непосредственно влиять на конформацию фермента, а также обеспечивать оптимальные условия для его работы, влияя на рН цитоплазмы как противоион протонов. Аналогично могут действовать и ионы калия. Магний активирует ряд реакций переноса электронов при фотофосфорилировании: восстановление NADP+, скорость реакции Хилла, он необходим при передаче электронов от ФС II к ФС I.
Действие магния на другие участки обмена веществ чаще всего связано с его способностью регулировать работу ферментов и значение его для ряда ферментов уникально. Только марганец может заменить магний в некоторых процессах. Однако в большинстве случаев активация ферментов магнием (в оптимальной концентрации) выше, чем марганцем.
Магний является кофактором почти всех ферментов, катализирующих перенос фосфатных групп (фосфокиназ, фосфо-трансфераз, АТРаз, пирофосфатаз). Это связано со способностью магния к комплексообразованию. Так, в реакциях с использованием в качестве субстрата АТР магний образует комплекс Mg-ATP, который затем связывается с каталитическим центром фермента:
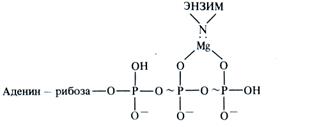
Аналогичный комплекс может образовываться и с ADP, хотя в этом случае сродство к магнию ниже и он может быть заменен марганцем. Помимо участия в переносе фосфора от одного соединения к другому магний также активирует ряд ферментов, катализирующих перенос фосфатной группы внутри одной молекулы (фосфоглюкомутаза и др.).
Магний необходим для многих ферментов гликолиза и цикла Кребса. В митохондриях при его недостатке наблюдается уменьшение количества, нарушение формы и в конечном счете исчезновение крист. Для девяти из двенадцати реакций гликолиза требуется участие металлов- активаторов и шесть из них активируются магнием.
Это четыре киназы (гексо-, фосфофрукто-, фосфоглицерат-, пируваткиназы), енолаза и пируваткарбоксилаза. За исключением фумаразы, все ферменты цикла Кребса активируются магнием или содержат его как интегральный компонент структуры. Для двух из семи ферментов пентозофосфатного пути (глюкозо-6-фосфатдегидро-геназа и транскетолаза) также необходим Mg. Он требуется и для работы ферментов молочнокислого и спиртового брожения.
Магний усиливает синтез эфирных масел, каучука, витаминов А и С. Предполагается, что, образуя комплексное соединение с аскорбиновой кислотой, он задерживает ее окисление. Mg2+ необходим для формирования рибосом и полисом, для активации аминокислот и синтеза белков (см. рис. 10.2) и используется для всех процессов в концентрации не менее 0,5 ммоль/л. Он активирует ДНК- и РНК-полимеразы, участвует в формировании определенной пространственной структуры нуклеиновых кислот.
При повышении степени обеспеченности магнием в растениях возрастает содержание органических и неорганических форм фосфорных соединений. Этот эффект, вероятно, связан с ролью магния в активации ферментов, участвующих в метаболизме фосфора.
Процесс поступления магния в растения может зависеть от степени обеспеченности растений другими катионами. Так, при высоком содержании калия или аммония в почве или в питательном растворе уровень магния, особенно в вегетативных частях растений, снижается. В плодах же количество магния при этом не меняется или может даже возрастать.
Наоборот, при низком уровне калия или аммония в питательной среде содержание магния в растении повышается. Кальций и марганец также действуют как конкуренты в процессе поглощения магния растениями. Токсическое действие избытка Мп:+ на растения можно уменьшить или даже снять высокими дозами магния. Соотношение Ca/Mg имеет большое значение для жизнедеятельности растений и регулирует многие процессы обмена веществ.
Недостаток в магнии растения испытывают в основном на песчаных почвах. Бедны магнием и кальцием подзолистые почвы, богаты — сероземы; черноземы занимают промежуточное положение. Водорастворимого и обменного магния в почве 3—10%. В почвенном поглощающем комплексе больше всего содержится ионов кальция, магний стоит на втором месте. Недостаток в магнии растения испытывают в тех случаях, когда его содержится менее 2 мг на 100 г почвы. При снижении рН почвенного раствора магний поступает в растения в меньших количествах.
Недостаток магния приводит к уменьшению содержания фосфора в растениях, даже если фосфаты в достаточных количествах имеются в питательном субстрате, тем более, что транспортируется фосфор по растению в основном в органической форме. Поэтому дефицит магния будет тормозить образование фосфорорганических соединений и соответственно распределение фосфора в растительном организме.
При недостатке магния накапливаются моносахариды, тормозится их превращение в полисахариды (в крахмал), слабо функционирует аппарат синтеза белка, рибосомы диссоциируют на субъединицы. Это приводит к увеличению в 1,5 — 4 раза количества свободных аминокислот. При недостатке магния нарушается формирование пластид: матрикс хлоропластов просветляется, граны слипаются. Ламеллы стромы разрываются и не образуют единой структуры, вместо них появляется много везикул. При магниевом голодании между зелеными жилками появляются пятна и полосы светло-зеленого, а затем желтого цвета. Края листовых пластинок приобретают желтый, оранжевый, красный или темно-красный цвет, и такая «мраморная» окраска листьев наряду с хлорозом служит характерным признаком нехватки магния. На более поздних стадиях магниевого голодания светло-желтые и беловатые полоски отмечаются и на молодых листьях, свидетельствуя о разрушении в них хлоропластов, а затем и каро-тиноидов, причем зоны листа, прилежащие к сосудам, дольше остаются зелеными. Впоследствии развиваются хлороз и некроз, затрагивая в первую очередь верхушки листьев.
Признаки магниевой недостаточности вначале проявляются на старых листьях, а затем распространяются на молодые листья и органы растения. Высокая и продолжительная освещенность усиливает признаки нехватки магния. Поскольку магний обладает сравнительно высокой подвижностью в растении, в некоторых случаях используют внекорневые подкормки — опрыскивание листьев.
 Железо. Среднее содержание железа в растениях составляет 0,02-0,08% (20-80 мг на 1 кг сухой массы). Fe3+ почвенного раствора восстанавливается редокс-системами плазма-леммы клеток ризодермы до Fe2+ и в такой форме поступает в корень.
Железо. Среднее содержание железа в растениях составляет 0,02-0,08% (20-80 мг на 1 кг сухой массы). Fe3+ почвенного раствора восстанавливается редокс-системами плазма-леммы клеток ризодермы до Fe2+ и в такой форме поступает в корень.
В составе соединений, содержащих гем (все цитохромы, каталаза, пероксидаза), и в негемовой форме (железосерные центры) железо принимает участие в функционировании основных редокс-систем фотосинтеза и дыхания. Вместе с молибденом железо участвует в восстановлении нитратов и в фиксации молекулярного азота клубеньковыми бактериями, входя в состав нитратредуктазы и нитрогеназы. Железо катализирует также начальные этапы синтеза хлорофилла (образование 8-аминолевулиновой кислоты и протопорфиринов). Поэтому недостаточное поступление железа в растения в условиях переувлажнения и на карбонатных почвах приводит к снижению интенсивности дыхания и фотосинтеза и выражается в пожелтении листьев (хлороз) и быстром их опадении.
Наряду с железом каталитичесци активных соединений ткани растений могут включать этот элемент в вещества запасного характера. Одно из них — белок ферритин, который содержит железо в негемовой форме. Он имеет оранжево-коричневую окраску и состоит из бесцветного белка апофер-ритина и нескольких тысяч атомов железа в виде соединений основного характера с гидроксильными и фосфатными группами. На долю железа может приходиться около 23% сухой массы ферритина. В больших количествах ферритин присутствует в пластидах.
Кремний обнаружен у всех растений. Особенно много его в клеточных стенках. Растения, накапливающие кремний, имеют прочные стебли. Диатомовые водоросли строят свои оболочки, концентрируя его из окружающей среды. Недостаток кремния может задерживать рост злаков (кукуруза, овес, ячменьХ и двудольных растений (огурцы, томаты, табак, бобы). Исключение кремния во время репродуктивной стадии вызывает уменьшение количества семян, при этом снижается число зрелых семян. При отсутствии в питательной среде кремния нарушается ультраструктура клеточных органелл.
Алюминий также относится к макроэлементам, в которых нуждаются только некоторые растения. Предполагается, что он имеет большое значение в обмене веществ у гидрофитов. Интересно отметить, что этот катион концентрируют папоротники и чай. При недостатке алюминия у чайного листа наблюдается хлороз, однако высокие концентрации токсичны для растений. В высоких дозах алюминий связывается в клетках с фосфором, что в итоге приводит к фосфорному голоданию растений.
 Микроэлементы представляют собой группу незаменимых минеральных элементов, выполняющих важные функции в жизнедеятельности растительных организмов. Их содержание в растениях составляет тысячные — стотысячные доли процента.
Микроэлементы представляют собой группу незаменимых минеральных элементов, выполняющих важные функции в жизнедеятельности растительных организмов. Их содержание в растениях составляет тысячные — стотысячные доли процента.
Микроэлементы принимают участие в окислительно-восстановительных процессах, фотосинтезе, азотном и углеводном обменах, входят в состав активных центров ферментов и витаминов, повышают устойчивость растений к болезням и неблагоприятным условиям внешней среды. Недостаток микроэлементов вызывает ряд заболеваний и нередко приводит к гибели растений уже в раннем возрасте.
Марганец необходим всем растениям. Среднее его содержание составляет 0,001 %, или 1 мг на 1 кг сухой массы тканей. В клетки он поступает в форме Мп2+. Марганец накапливается в листьях. Установлено участие ионов этого металла в выделении кислорода (фоторазложение воды) и восстановлении СОт при фотосинтезе. Марганец способствует увеличению содержания Сахаров и их оттоку из листьев. Две дегидрогеназы дыхательного цикла Кребса — малат- и изоцит-ратдегидрогеназы — активируются ионами марганца. Азотный обмен растений также не обходится без марганца, который необходим для функционирования комплекса нитратредуктазы при восстановлении нитратов.
 Марганец существен для процессов роста клеток, с одной стороны, как кофактор РНК-полимеразы II, ответственной за синтез мРНК в ядре, а с другой — необходим в качестве кофактора ауксиноксидазы — ферментативного комплекса, разрушающего ИУК. При исключении марганца из питательной среды в тканях растений возрастает уровень основных элементов минерального питания, нарушается их соотношение. Несмотря на значительное содержание марганца в почве, большая его часть труднодоступна для растений, особенно на почвах, имеющих нейтральные значения рН.
Марганец существен для процессов роста клеток, с одной стороны, как кофактор РНК-полимеразы II, ответственной за синтез мРНК в ядре, а с другой — необходим в качестве кофактора ауксиноксидазы — ферментативного комплекса, разрушающего ИУК. При исключении марганца из питательной среды в тканях растений возрастает уровень основных элементов минерального питания, нарушается их соотношение. Несмотря на значительное содержание марганца в почве, большая его часть труднодоступна для растений, особенно на почвах, имеющих нейтральные значения рН.
Чувствительны к недостатку марганца корнеплоды, картофель, злаковые. Характерный симптом марганцевого голодания — точечный хлороз листьев: между жилками появляются желтые пятна, а затем ткани в этих участках отмирают.
Наибольшее содержание молибдена характерно для бобовых (0,5 — 20 мг на кг сухой массы), злаки содержат от 0,2 до 2,0 мг молибдена на 1 кг сухой массы. Он поступает в растения как анион МоО-2, концентрируется в молодых, растущих органах. Его больше в листьях, чем в корнях и стеблях, а в листе сосредоточен в основном в хлоропластах.
 Молибден принимает участие в восстановлении нитратов, входя в состав нитратредуктазы, а также является компонентом активного центра нитрогеназы бактероидов, фиксирующих атмосферный азот в клубеньках бобовых.
Молибден принимает участие в восстановлении нитратов, входя в состав нитратредуктазы, а также является компонентом активного центра нитрогеназы бактероидов, фиксирующих атмосферный азот в клубеньках бобовых.
При недостатке Мо в тканях накапливается большое количество нитратов, не развиваются клубеньки на корнях бобовых, тормозится рост растений, наблюдается деформация листовых пластинок. Молибден, как и железо, необходим для биосинтеза легоглобина (леггемоглобина) — белка-переносчика кислорода в клубеньках бобовых. При дефиците молибдена клубеньки приобретают желтый или серый цвет, нормальная же их окраска — красная.
Как металл-активатор молибден необходим в реакциях аминирования и переаминирования, для включения аминокислот в пептидную цепь, работы таких ферментов, как ксан-тиноксидаза, и различных фосфатаз. Он оказывает влияние на уровень накопления аскорбиновой кислоты. При его недостатке наблюдается резкое снижение содержания в тканях этого витамина.
К присутствию молибдена в доступной форме особенно требовательны бобовые и овощные культуры. Недостаток его чаще встречается на кислых почвах, в которых он малоподвижен. При дефиците молибдена тормозится рост и из-за нарушения синтеза хлорофилла растения выглядят бледно-зелеными. Эти признаки похожи на признаки недостатка азота. Высокие дозы этого микроэлемента токсичны для растений. Значительное содержание молибдена в сельскохозяйственной продукции вредно и для животных, и для человека. Если содержание Мо в растениях достигает 20 мг и более на 1 кг сухой массы, у животных при употреблении свежих растений наблюдаются молибденовые токсикозы, а у человека — эндемическая подагра.
 Среднее содержание кобальта в растениях — 0,00002 %, или 0,02 мг на 1 кг сухой массы. Кобальт необходим бобовым растениям для обеспечения размножения клубеньковых бактерий. В растениях кобальт встречается в ионной форме и в пор-фириновом соединении — витамине B12. Растения, как и животные, не синтезируют витамина В12 (В12-коэнзим). Он вырабатывается бактероидами клубеньков бобовых растений и участвует в синтезе метионина в бактероидах, фиксирующих азот. При старении клубеньков и прекращении фиксации азота В12-коэнзим выходит в цитоплазму клеток клубеньков.
Среднее содержание кобальта в растениях — 0,00002 %, или 0,02 мг на 1 кг сухой массы. Кобальт необходим бобовым растениям для обеспечения размножения клубеньковых бактерий. В растениях кобальт встречается в ионной форме и в пор-фириновом соединении — витамине B12. Растения, как и животные, не синтезируют витамина В12 (В12-коэнзим). Он вырабатывается бактероидами клубеньков бобовых растений и участвует в синтезе метионина в бактероидах, фиксирующих азот. При старении клубеньков и прекращении фиксации азота В12-коэнзим выходит в цитоплазму клеток клубеньков.
Наряду с магнием и марганцем кобальт активирует фермент гликолиза фосфоглюкомутазу и фермент, осуществляющий гидролиз аргинина, — аргиназу.
Внешние признаки недостатка кобальта у бобовых сходны с признаками азотного голодания.
 Среднее содержание меди в растениях 0,0002%, или 0,2 мг на 1 кг массы, и зависит от видовых особенностей и почвенных условий. В растительную клетку медь поступает в форме Сu2+. В клетке 2/3, меди может находиться в нерастворимом, связанном состоянии. Относительно богаты этим элементом семена и растущие части. Около 70% всей меди, находящейся в листьях, сконцентрировано в хлоропластах и почти половина — в составе пластоцианина, осуществляющего перенос электронов между ФС II и ФС I. Она входит в состав медьсодержащих белков и ферментов, катализирующих окисление аскорбиновой кислоты, дифенолов и гидроксилирование монофенолов — аскорбатоксидазы, полифенолоксидазы, ортодифенолоксидазы и тирозиназы. Два атома меди функционируют в цитохромоксидазном комплексе дыхательной цепи митохондрий.
Среднее содержание меди в растениях 0,0002%, или 0,2 мг на 1 кг массы, и зависит от видовых особенностей и почвенных условий. В растительную клетку медь поступает в форме Сu2+. В клетке 2/3, меди может находиться в нерастворимом, связанном состоянии. Относительно богаты этим элементом семена и растущие части. Около 70% всей меди, находящейся в листьях, сконцентрировано в хлоропластах и почти половина — в составе пластоцианина, осуществляющего перенос электронов между ФС II и ФС I. Она входит в состав медьсодержащих белков и ферментов, катализирующих окисление аскорбиновой кислоты, дифенолов и гидроксилирование монофенолов — аскорбатоксидазы, полифенолоксидазы, ортодифенолоксидазы и тирозиназы. Два атома меди функционируют в цитохромоксидазном комплексе дыхательной цепи митохондрий.
Определенные функции выполняет этот микроэлемент в азотном обмене, входя в состав нитратредуктазного комплекса. Он влияет на синтез легоглобина и активность ряда ферментов, участвующих в фиксации молекулярного азота атмосферы.
За счет инактивирования ауксинов полифенолоксидазой медь снижает ингибирующее действие на рост высоких доз этих ростовых веществ. Для биосинтеза этилена также необходим медьсодержащий фермент. По-видимому, благодаря регулирующему действию на содержание в растениях ингибиторе роста фенольной природы медь повышает устойчивость растений к полеганию. Она повышает также засухо-, морозо- и жароустойчивость.
Недостаток меди вызывает задержку роста и цветения, хлороз, потерю тургора и завядание растений. У злаков при остром дефиците меди белеют кончики листьев и не развивается колос, у плодовых появляется суховершинность.
Содержание цинка в надземных частях бобовых и злаковых растений составляет 15 — 60 мг на 1 кг сухой массы. Повышенная концентрация отмечается в листьях, репродуктивных органах и конусах нарастания, наибольшая — в семенах.
 Цинк поступает в растение в форме катиона Zn2+, оказывая многостороннее действие на обмен веществ. Он необходим для функционирования ряда ферментов гликолиза — гексокиназы, енолазы, триозофосфатдегидрогеназы, альдолазы, а также входит в состав алкогольдегидрогеназы. Цинк активирует карбоангидразу, катализирующую реакцию дегидратации гидрата оксида углерода: Н2СО3 ↔ СО2 + Н2О, что помогает использованию СО2 в процессе фотосинтеза.
Цинк поступает в растение в форме катиона Zn2+, оказывая многостороннее действие на обмен веществ. Он необходим для функционирования ряда ферментов гликолиза — гексокиназы, енолазы, триозофосфатдегидрогеназы, альдолазы, а также входит в состав алкогольдегидрогеназы. Цинк активирует карбоангидразу, катализирующую реакцию дегидратации гидрата оксида углерода: Н2СО3 ↔ СО2 + Н2О, что помогает использованию СО2 в процессе фотосинтеза.
Роль цинка важна также в образовании аминокислоты триптофана. Именно с этим связано влияние Zn2+ на синтез белков, а также фитогормона индолилуксусной кислоты (ауксина), предшественником которой является триптофан. Подкормка цинком способствует увеличению содержания ауксинов в тканях и активирует их рост.
При дефиците цинка у растений нарушается фосфорный обмен: фосфор накапливается в корневой системе, задерживается его транспорт в надземные органы, замедляется' превращение фосфора в органические формы — в несколько раз возрастает содержание неорганических фосфатов, снижается содержание фосфора в составе нуклеотидов, липидов и нуклеиновых кислот.
После добавления цинка фосфорный обмен у растений нормализуется.
При недостатке цинка в растениях накапливаются редуцирующие сахара и уменьшается содержание сахарозы и крахмала, увеличивается количество органических кислот и небелковых соединений азота — амидов и аминокислот. Кроме того, в 2 — 3 раза подавляется скорость деления клеток, что приводит к морфологическим изменениям листьев, нарушению растяжения клеток и дифференциации тканей.
Весьма чувствительны к цинку плодовые деревья, особенно цитрусовые. Наиболее характерный признак цинкового голодания — задержка роста междоузлий и листьев, появление хлороза и развитие розеточности.
 Бор — один из наиболее важных для растений микроэлементов. Его среднее содержание составляет 0,0001 %, или 0,1 мг на 1 кг сухой массы. В боре наиболее нуждаются двудольные растения. Обнаружено значительное содержание бора в цветках, особенно в рыльце и столбиках. В клетке большая часть этого микроэлемента сконцентрирована в клеточных стенках. Бор усиливает рост пыльцевых трубок, прорастание пыльцы, увеличивает количество цветков и плодов. Без него нарушается созревание семян. Бор снижает активность некоторых дыхательных ферментов, оказывает влияние на углеводный, белковый и нуклеиновый обмен. При его недостатке нарушаются синтез, превращения и транспорт углеводов, формирование репродуктивных органов, оплодотворение и плодоношение. Бор необходим растениям в течение всего периода их развития. Он не может реутилизироваться и поэтому при борном голодании прежде всего отмирают конусы нарастания — наиболее типичный симптом борной недостаточности.
Бор — один из наиболее важных для растений микроэлементов. Его среднее содержание составляет 0,0001 %, или 0,1 мг на 1 кг сухой массы. В боре наиболее нуждаются двудольные растения. Обнаружено значительное содержание бора в цветках, особенно в рыльце и столбиках. В клетке большая часть этого микроэлемента сконцентрирована в клеточных стенках. Бор усиливает рост пыльцевых трубок, прорастание пыльцы, увеличивает количество цветков и плодов. Без него нарушается созревание семян. Бор снижает активность некоторых дыхательных ферментов, оказывает влияние на углеводный, белковый и нуклеиновый обмен. При его недостатке нарушаются синтез, превращения и транспорт углеводов, формирование репродуктивных органов, оплодотворение и плодоношение. Бор необходим растениям в течение всего периода их развития. Он не может реутилизироваться и поэтому при борном голодании прежде всего отмирают конусы нарастания — наиболее типичный симптом борной недостаточности.
 Согласно концепции М. Я. Школьника неметалл бор в отличие от микроэлементов-металлов не является компонентом или активатором ферментов и характеризуется специфической ролью в жизнедеятельности растений благодаря своей уникальной роли в фенольном обмене. Предполагается, что при недостатке бора в клетках двудольных растений накапливаются фенолы и супероптимальные концентрации ауксинов, что нарушает синтез нуклеиновых кислот и белков; затем нарушаются ритм деления клеток и структура клеточных стенок, появляются тератологические (уродливые) изменения в формирующихся листьях конуса нарастания. На заключительной стадии борного голодания под влиянием накапливающихся фенольных соединений возрастает проницаемость тонопласта для полифенолов. Полифенолы выходят из вакуоли в цитоплазму и окисляются полифенолоксидазой до токсичных веществ типа хинонов, которые отравляют растения, приводя к отмиранию конусов нарастания.
Согласно концепции М. Я. Школьника неметалл бор в отличие от микроэлементов-металлов не является компонентом или активатором ферментов и характеризуется специфической ролью в жизнедеятельности растений благодаря своей уникальной роли в фенольном обмене. Предполагается, что при недостатке бора в клетках двудольных растений накапливаются фенолы и супероптимальные концентрации ауксинов, что нарушает синтез нуклеиновых кислот и белков; затем нарушаются ритм деления клеток и структура клеточных стенок, появляются тератологические (уродливые) изменения в формирующихся листьях конуса нарастания. На заключительной стадии борного голодания под влиянием накапливающихся фенольных соединений возрастает проницаемость тонопласта для полифенолов. Полифенолы выходят из вакуоли в цитоплазму и окисляются полифенолоксидазой до токсичных веществ типа хинонов, которые отравляют растения, приводя к отмиранию конусов нарастания.
 2015-05-26
2015-05-26 2505
2505
