С электропроводностью растворов солей в воде связано очень многое в нашей жизни.
С первого удара сердца (“живое” электричество в теле человека, на 80% состоящем из воды) до автомобилей на улице, плееров и мобильных телефонов (неотъемлемой частью этих устройств являются “батарейки” - электрохимические элементы питания и различные аккумуляторы - от свинцово-кислотных в автомобилях до литий-полимерных в самых дорогих мобильных телефонах”. В огромных, дымящихся ядовитыми парами чанах из расплавленного при огромной температуре боксита электролизом получают алюминий - “крылатый” металл для самолетов и банок для “фанты”. Все вокруг - от хромированной решетки радиатора иномарки до посеребренной сережки в ухе когда-либо сталкивалось с раствором или расплавом солей. А, следовательно, с электрическим током в жидкостях. Не зря это явление изучает целая наука - электрохимия, но нас сейчас больше интересуют физические основы этого явления
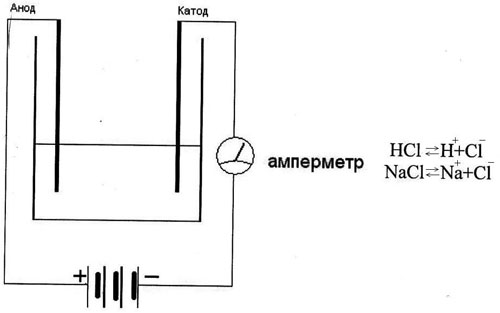
2. Демонстрация опыта:
Дистилированная вода не проводит ток в собранной установке. Лампочка не загорается, а если добавим в эту воду немного кислоты или соли, то в цепи появится ток и лампочка загорит. Происходит распад молекулы на (+) и (-) ионы, электролитическая диссоциация (связь с химией).
“Атомы вещества каким-то образом одарены электрическими силами или связаны с ними, и им они обязаны своими наиболее замечательными качествами.” (М. Фарадей)
Вывод: электронная и ионная проводимость растворов
 2015-05-26
2015-05-26 286
286







