1 Изучить установку для исследования процесса кристаллизации сплава термическим методом и зарисовать ее схему.
2 Исследовать процесс кристаллизации заданного преподавателем сплава, внести данные по изменению температуры во времени в таблицу, построить кривую охлаждения (с применением правила Гиббса и пояснением фазовых превращений).
3 После сведения результатов в таблицу по каждому исследованному сплаву построить диаграмму состояния изучаемой системы.
4 Определить с помощью правила отрезков фазы и их содержание для заданной преподавателем температуры сплава.
Лабораторная работа № 6. Анализ диаграмм состояния двойных сплавов
Цель работы: изучить основные типы диаграмм состояния двойных систем; приобрести практические навыки изучения превращений, протекающих при кристаллизации сплавов; проанализировать полученные данные и определить возможность их использования на практике.
Учение о равновесных диаграммах металлических систем, характеризующих различные состояния сплавов в зависимости от температуры и состава, имеет большое значение.
Умея читать диаграмму состояния, можно представить полную картину образования сплава, его переход из жидкого состояния в твердое, процессы перекристаллизации в твердом состоянии; можно определить оптимальную температуру заливки сплава, оценить его жидкотекучесть, определить склонность к ликвации.
Еще большее значение диаграммы состояния имеют для термической обработки сплавов. В этом случае по ним можно определить какую тепловую обработку может воспринимать данный сплав и какие температурные режимы будут для него наиболее рациональными.
Таким образом, диаграммы состояния двойных и более сложных систем показывают графически, как с изменением химического состава и температуры изменяются структура, количество и состав фаз, находящихся в равновесии.
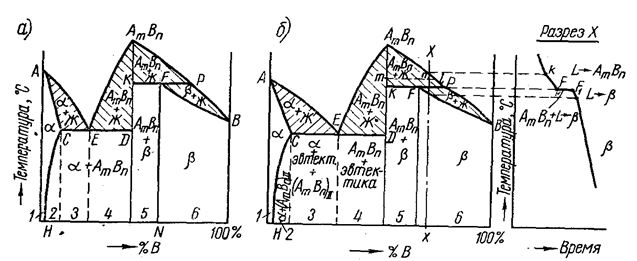
а – фазовый анализ: б – структурный анализ
Рисунок 6.1 – Диаграмма состояния для металлов А и В
Любая точка диаграммы состояния сплавов показывает:
─ температуру сплава;
─ фазовый состав сплава;
─ структуру сплава.
В качестве примера на рисунке 6.1 приведена диаграмма состояния для металлов А и В.
Из диаграммы видно, что выше заштрихованных областей (выше линии ликвидуса) сплавы находятся в жидком состоянии; ниже заштрихованных областей (ниже линии солидуса) сплавы находятся в твердом состоянии.
В заштрихованных областях присутствуют две фазы (жидкая и кристаллы твердой фазы).
Два металла А и В (компоненты) могут образовывать в рассматриваемой системе фазы, указанные по областям на рисунке 6.1, а:
- химическое соединение определенного состава, которое может быть выражено формулой АтВп, где m и n простые целые числа;
- твердые растворы a и b, где a – твердый раствор на основе компонента А – область 1 и b – твердый раствор на основе компонента В – область 6.
Перечисленные фазы могут находиться как в структурно-свободном состоянии, так и в различном сочетании друг с другом, образуя механические смеси.
Одинаковый фазовый состав имеют области 2, 3 и 4: a -твердый раствор и АтВп; но структурно они сочетаются различно в зависимости от химического сплава, как это показано на рисунке 6.1, б.
Предельная растворимость компонентов В и А определяется линией СН.
Из диаграммы видно, что с понижением температуры растворимость металлов В и А уменьшается.
На линии CED происходит эвтектическое превращение: жидкий сплав (состава точки Е) превращается в механическую смесь – эвтектику (кристаллы a -твердого раствора точки С + кристаллы АтВп точки D):
LЕ ® [aC + АmВn ].
Эвтектические сплавы являются более легкоплавкими, чем все остальные сплавы данной системы.
На горизонтальной линии KFP происходит перитектическое превращение. Оно заключается в том, что здесь кристаллы АтВп путем взаимодействия с окружающей их жидкостью образуют кристаллы твердого раствора.
Это превращение можно выразить так:
АmВn + LP ® bF.
В некоторых областях диаграммы структурный состав будет отличаться от фазового состава.
В области 2 сплавы состоят из кристалловa-твердого раствора и некоторого количества вторичных кристаллов АтВп, выделившихся из a-твердого раствора.
Доэвтектические сплавы – область 3 – по структуре состоят из кристаллов a -твердого раствора + эвтектика + АтВп (вторичные кристаллы).
Заэвтектические сплавы – область 4 – по структуре состоят из кристаллов АтВп (первичные) + эвтектика.
Вследствие перитектического превращения сплавы в зависимости от их состава могут приобретать различную структуру. Если сплавы по составу находятся между точками К и F (область 5), структура состоит из кристаллов АтВп + b -твердый раствор (механическая смесь). Если сплавы лежат между точками F и Р (область 6), будет образовываться одна фаза – b - твердый раствор.
Таким образом, структурный анализ этих областей не будет отличаться от фазового состава.
Применяя правило отрезков, можно количественно определить сколько имеется процентов той или другой фазы по отношению к общему весу сплава.
Для определения состава и количества фаз в заданном сплаве Х (см. рисунок 6.1, б) при заданной температуре (точка n) нужно провести горизонталь через точку n до пересечения с ближайшими линиями диаграммы; точки пересечения т и l будут определять составы фаз, а длины отрезков на проведенной горизонтали дадут соотношения, пропорциональные количеству (весу) фаз.
Для сплава Х при заданной температуре – по линии mnl
количество жидкой фазы/ количество всего сплава = mn/ml.
Можно сказать, что отношение длины малого отрезка тп к большому ml таков же, как отношение веса жидкой фазы сплава к весу всего сплава.
Можно определить и количество выделившейся твердой фазы АтВп. Оно составит такую часть всего сплава, какую часть большего отрезка ml составляет малый отрезок п1:
количество АтВп / количество всего сплава = nl/ml
Таким образом, если в сплаве одновременно присутствуют две фазы, то с помощью правила отрезков можно определить процентное количество как одной, так и другой фазы.
Количественное отношение между весом твердой фазы АтВп и весом жидкой фазы для сплава Х будет следующее:
вес жидкой фазы/ вес твердой фазы = mn/п1
 2015-05-26
2015-05-26 757
757








