Большее применение в производстве радиоэлектронных средств получили различные сплавы - материалы, образованные путем соединения в жидком, расплавленном состоянии двух или более различных элементов между собой. Строение сплавов более сложное, чем чистых элементов, и зависит от того, в какие взаимодействия вступают составляющие компоненты. Сплавы могут представлять собой механическую смесь, химические соединения и твердые растворы.
3.1. Механическая смесь
Механическая смесь образуется тогда, когда компоненты А и В не способны к взаимному растворению в твердом состоянии и не вступают в химическую реакцию с образованием соединения. Сплав будет состоять из отдельных зерен кристаллов компонентов А и В, отчетливо выявленных на микроструктуре (рис. 3.1).
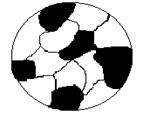
Рис. 3.1. Микроструктура механической смеси (схема)
Механические свойства сплава зависят от размеров и форм зерен, количественного соотношения компонентов и занимают промежуточное положение между соответствующими параметрами чистых компонентов.
3.2. Твердые растворы
Твердые растворы - это сплавы, в которых один из компонентов (растворитель) сохраняет свою кристаллическую решетку, а атомы другого компонента (растворимого) располагаются в решетке первого, изменяя ее размеры (периоды). Таким образом, твердый раствор, состоящий из двух или более компонентов, имеет один тип кристаллической решетки и представляет собой одну фазу. Фазой называют однородные гомогенные составные части системы, имеющие одинаковый состав, кристаллическое строение и свойства, одно и то же агрегатное состояние и отделены от составных частей поверхностями раздела, при переходе через которые химический состав или структура вещества изменяются скачками.
Химический или спектральный анализ может показывать в твердом растворе наличие двух или более компонентов, тогда как по данным металлографического анализа такой сплав, как и чистый металл, имеет однородные зерна (рис. 3.2).
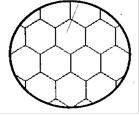
Рис. 3.2. Микроструктура твердого раствора (схема)
Различают твердые растворы замещения и твердые растворы внедрения (рис. 3.3, а, б). В твердых растворах замещения атомы растворенного компонента В частично замещают атомы в решетке основного элемента А (рис. 3.3, а).
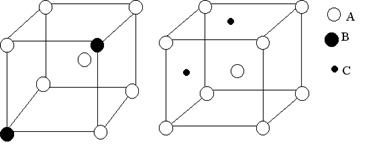
а) б)
Рис. 3.3. Схема твердого раствора замещения (а) и твердого раствора внедрения (б)
При образовании твердых растворов замещения периоды решетки изменяются в зависимости от разности диаметров атомов растворителя А и растворенного элемента В. Если атом В больше атома А, то элементарная ячейка увеличивается, если меньше, то сокращается. Независимо от видов элементов, входящих в твердый раствор, изменение параметров решетки обусловливает изменение различных свойств сплавов, например, прочности; при этом уменьшение размера решетки приводит к большему упрочнению, чем при расширении.
Твердые растворы замещения могут быть ограниченные и неограниченные. При ограниченной растворимости только до определенного количества атомы элемента В могут замещать атомы растворителя А в кристаллической решетке. Например, в сплаве Al-Cu может растворяться до 5,7 % Cu в алюминии, в сплаве Cu-Zn до 39 % Zn в меди без изменения их кристаллической решетки. При неограниченной растворимости любое количество атомов А может быть заменено атомами В, т.е. образуется непрерывный ряд твердых растворов. Неограниченные твердые растворы могут образоваться при соблюдении следующих условий:
наличие в обоих компонентах одинаковых по типу (изоморфных) кристаллических решеток;
небольшое различие в атомных размерах компонентов (DR не должна превышать 8-15 %);
компоненты сплава должны близко располагаться в периодической таблице Д.И. Менделеева, т. е. близкими по строению валентной оболочке атомов, по физической природе.
Например, неограниченный ряд твердых растворов образуется в сплавах, компоненты которых имеют ГЦК-решетку: Au-Ag (DR = 0,2 %), Ni-Cu (DR = 2,7 %) и др.; в сплавах с ОЦК-решеткой: Мо-W (DR = 9,9%), V-Ti(DR = 2 %). Если элементы не отвечают перечисленным выше условиям, то они ограниченно растворяются друг в друге. Ограниченная растворимость почти всегда уменьшается с понижением температуры.
В твердых растворах внедрения атомы растворенного компонента С (рис. 3.3, б), располагаются в междоузлиях (пустотах) кристаллической решетки растворителя А. В данном случае размеры атомов компонентов, входящих в сплав могут и должны отличаться по величине, а кристаллическая решетка компонента растворителя должна давать возможность размещения дополнительных атомов. Твердые растворы этого типа возникают в тех случаях, когда диаметр атома растворенного элемента невелик, а внутри решетки растворителя А должно иметься достаточное количество пространства для атома С. Твердые растворы внедрения возникают при растворении в металлах (Fe, Cr, Mo) элементов с малым радиусом: углерода (атомный радиус 0,077 нм), азота (0,071 нм), водорода (0,046 нм), например, при образовании сталей.
Твердые растворы внедрения могут быть только ограниченной концентрации, так как число пор в решетке ограничено, а атомы основного компонента сохраняются в узлах решетки. Как указывалось выше, при образовании твердых растворов замещения период решетки может увеличиваться или уменьшатся в зависимости от соотношения размеров атомов растворителя или растворенного компонента, в случае твердых растворов внедрения период решетки растворителя всегда возрастает. Атомы растворенного компонента нередко скапливается у дислокаций, снижая их упругую энергию. В области дислокаций атомы внедрения легче размещаются, чем в совершенной кристаллической решетке, где они могут вызывать значительные искажения. При этом они сильнее связываются с дислокациями, чем атомы замещения, образуя так называемые атмосферы Коттрелла. Образование атмосфер увеличивает устойчивость структуры сплава, так как искажение решетки снижается.
Ряд сплавов при достаточно высоких температурах образует твердые растворы замещения (Fe-Si, Cu-Au, Fe-Al) c неупорядоченным расположением элементов. Однако при медленном охлаждении происходит перераспределение в расположении компонентов, и они занимают определенные места в узлах решетки, т.е. происходит упорядочение структуры. Такие сплавы называют упорядоченными твердыми растворами или сплавами со сверхструктурой. Упорядочение структуры сопровождается изменением физических (электрические, магнитные) и механических свойств, при этом прочность возрастает, а пластичность падает. Упорядоченные твердые растворы являются промежуточными фазами между твердыми растворами и химическими соединениями, однако, в отличие от химических соединений, в них сохраняется кристаллическая решетка растворителя. В сплавах, содержащих более двух элементов, возможны твердые растворы сложного состава - замещения и внедрения. Например, в сплавах железа с углеродом и марганцем получается твердый раствор, в котором углерод растворяется путем внедрения, а марганец - замещения.
Химические соединения - структура сплава, образованная компонентами его, взаимодействующими между собой в соответствии со стехиометрическими законами. Химические соединения обладают рядом особенностей:
образуется специфическая кристаллическая решетка с упорядоченным расположением атомов, отличная от решетки компонентов, входящих в химическое соединение;
соотношение чисел атомов соответствует кратному соотношению компонентов, входящих в химическое соединение, что может быть выражено простой формулой АnВm;
определенная температура плавления (диссоциации) и скачкообразное изменение свойств при изменении состава (так называемой сингулярностью свойств).
Химические соединения обычно образуются из компонентов сплава, имеющих большое различие в размерах атомов, в электронном строении их и кристаллических решеток. Структура химических соединений зависит от следующих факторов: относительного размера атомов, их валентности и от положения в периодической системе элементов, что и определяет строение электронной оболочки.
Химические соединения могут быть образованы только металлическими элементами; в этом случае связь металлическая. Она не является жесткой и поэтому при определенных условиях количество элементов, входящих в соединение может быть различными и может отличаться от стехиометрического состава. Соединение одних металлов с другими носят общее название интерметаллидов или интерметаллических соединений.
При образовании химических соединений металла с неметаллом возникает ионная связь. В этом случае атом металла отдает валентные электроны и становится положительным ионом, а атом металлоида принимает электроны и становится отрицательным ионом. В соединениях такого типа связь жесткая, химический состав постоянный и соответствует стехиометрическому соотношению. Такие химические соединения подчиняются закону валентности. В настоящее время известно большое число различных химических соединений при образовании сплавов, которые отличаются спецификой формирования структур и особыми свойствами. Рассмотрим наиболее важные химические соединения, образующиеся в сплавах.
Электронные соединения. Электронные соединения характеризуются тем, что в них существует определенное отношение валентных электронов к числу атомов элементов, входящих в сплав (3/2; 21/13; 7/4). Этот вид соединений образуется между одновалентными металлами (Сu, Ag, Au, Li, Na) или металлами переходных групп (Fe, Mo, Ni и др.) с одной стороны и элементами валентностью от 2 до 5 (Be, Zn, Cd, Al, Sn, Si, Mg) - c другой. Каждому отношению валентных электронов к числу атомов соответствует определенная кристаллическая решетка. Так при соотношении 3/2 образуется ОЦК решетка (так называемая b - фаза), при соотношении 21/13 - сложная кубическая решетка с 52 атомами на ячейку (так называемая g - фаза) и при соотношении 7/4 соединение имеет плотноупакованную гексагональную решетку (e - фаза). В таблице приведены наиболее важные технические сплавы с электронными соединениями.
У электронных соединений, как указывалось выше, существует определенное соотношение атомов, и они имеют кристаллическую решетку, отличную от решетки компонентов входящих в сплав - это признаки, характерные для химических соединений. При высоких температурах часто нарушается упорядочение в расположении атомов, они располагаются статистически, при понижении температуры до определенного значения происходит упорядочение. Поэтому многие авторы считают, что электронные соединения являются промежуточными между химическим и твердым раствором.
 2015-05-26
2015-05-26 6580
6580
