В соответствии с разделением окислительно-восстановительной реакции на две полуреакции, электродвижущие силы также принято представлять в виде разности двух величии, каждая из которых отвечает данной полуреакции. Эти величины называются электродными потенциалами.
Если из всего ряда стандартных электродных потенциалов выделить только те электродные процессы, которые отвечают общему уравнению Мz+ + zе = М то получим ряд напряжений металлов. В этот ряд всегда помещают, кроме металлов, также водород, что позволяет видеть, какие металлы способны вытеснять водород из водных растворов и кислот.
Св-ва ряда напряжений: -в начале ряда Ме наиболее химически активны;
-в конце наиболее химически инертные;
-Ме может вытеснять след. Ме из р-ра солей;
-Ме до Мg могут вытеснять из воды водород при обычных условиях;
-Ме от Мg включ. до Н вытесняют водород из воды при опред. условиях;
-все Ме до Н вытесняют Н 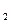 из разбавленных растворов кислот, за исключением азотной к-ты(все Ме с НNО
из разбавленных растворов кислот, за исключением азотной к-ты(все Ме с НNО 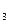 реагируют без выделения Н
реагируют без выделения Н 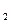 );
);
-Ме после Н водород не вытесняют.
 2015-05-30
2015-05-30 739
739








