Патогенные агенты вызывают нарушение функций клеток. В табл. 5–1 приводятся наиболее важные механизмы клеточной альтерации.
Ы Вёрстка Таблица 5‑1 большая, но её надо уместить на одной странице: это вполне возможно вместе с параграфом, где отсылка (если параграф с отсылкой на нечётной странице, а таблица на чётной следующего разворота, то к отсылке добавить «(см. на следующей странице)»).
Таблица 5–1. Основные механизмы повреждения клетки
| 1. Расстройства энергетического обеспечения клетки – Снижение интенсивности и/или эффективности ресинтеза АТФ – Нарушение механизмов транспорта энергии АТФ – Расстройство механизмов использования энергии АТФ 2. Повреждение мембран и ферментов клетки – Чрезмерное образование активных форм кислорода, интенсификация свободнорадикальных реакций и СПОЛ – Значительная активация гидролаз (лизосомальных, мембраносвязанных, свободных). – Внедрение амфифильных соединений в липидную фазу мембран и их детергентное действие – Торможение ресинтеза повреждённых компонентов мембран и/или синтеза их de novo – Нарушение конформации макромолекул белка, ЛП, фосфолипидов – Перерастяжение и разрыв мембран набухших клеток и/или их органелл Дисбаланс ионов и воды в клетке – Изменение соотношения отдельных ионов в цитозоле – Нарушение трансмембранного соотношения ионов – Гипергидратация клеток – Гипогидратация клеток – Нарушения электрогенеза Нарушения в геноме и/или механизмов экспрессии генов –Мутации –Дерепрессия патогенных генов –Репрессия жизненно важных генов –Трансфекция (внедрение в геном чужеродной ДНК) –Дефекты транскрипции, процессинга, трансляции, посттрансляционной модификации –Дефекты репликации и репарации –Нарушение митоза и мейоза Расстройства регуляции функций клеток –Нарушение рецепции регулирующих воздействий –Образование вторых посредников –Расстройства регуляции метаболических процессов в клетке |
Расстройства энергетического обеспечения клетки
Энергетическое обеспечение клеток осуществляется за счёт АТФ, образующейся преимущественно в процессе окислительного фосфоридирования в митохондриях и в меньшей мере – в реакциях гликолиза в цитозоле.
Энергоснабжение клетки может расстраиваться на любом из этапов: ресинтеза, транспорта и утилизации энергии АТФ (рис. 5–2).
Ы ВЁРСТКА вставить файл «ПФ Рис 05 02 Hарушения энергообеспечения клетки при ее повреждении»
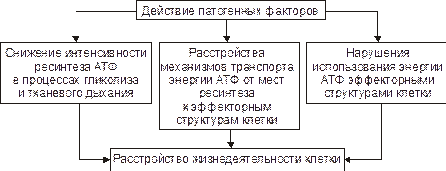
Рис. 5–2. Механизмы нарушения энергообеспечения в повреждённой клетке.
Нарушения ресинтеза АТФ. Ресинтез АТФ может расстраиваться в результате дефицита кислорода и/или субстратов метаболизма, снижения активности ферментов тканевого дыхания и гликолиза, повреждения и разрушения митохондрий, в которых осуществляются реакции цикла Кребса и перенос электронов к молекулярному кислороду, сопряжённый с фосфорилированием АДФ.
Расстройства транспорта энергии. Заключённая в макроэргических связях энергия АТФ в норме доставляется от мест ресинтеза – митохондрий и цитозоля – к эффекторным структурам (миофибриллам, мембранным ионным насосам и др.) с помощью АДФ‑АТФ‑транслоказы (адениннуклеотидилтрансферазы) и КФК. Адениннуклеотидилтрансфераза обеспечивает транспорт энергии макроэргической фосфатной связи АТФ из матрикса митохондрий через их внутреннюю мембрану, а КФК переносит её далее на креатин с образованием креатинфосфата, который поступает в цитозоль (рис. 5–3). КФК эффекторных клеточных структур транспортирует фосфатную группу креатинфосфата на АДФ с образованием АТФ, который и используется в процессах жизнедеятельности клетки.
Ы ВЁРСТКА вставить файл «ПФ Рис 05 03 Механизм транспорта энергии»
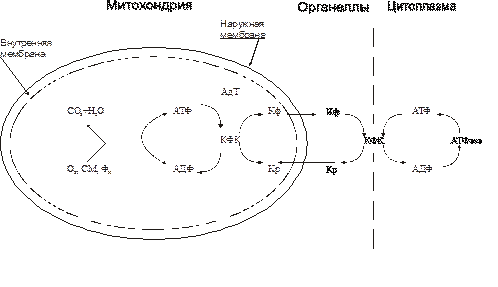
Рис. 5–3. Механизм транспорта энергии АТФ в клетке. АдТ – адениннуклеотидилтрансфераза; Кр – креатин; Кф – креатинфосфат; СМ – субстраты метаболизма; ФН – фосфат неорганический.
Системы транспорта энергии могут быть повреждены различными патогенными агентами, в связи с чем (даже на фоне высокого общего содержания АТФ в клетке) может развиваться дефицит АТФ в энергорасходующих структурах.
Расстройство утилизации энергии. Нарушения энергообеспечения клеток и расстройства их жизнедеятельности могут развиваться в результате повреждения механизмов утилизации энергии, главным образом за счёт уменьшения активности АТФаз (АТФаза миозина, Na+,K+‑АТФаза плазмолеммы, протонная и калиевая АТФаза, Са2+‑АТФаза [Са2+‑насос] и др.). Следовательно, расстройство жизнедеятельности клеток может развиваться даже в условиях нормального или повышенного содержания в клетке АТФ.
Нарушение энергообеспечения, в свою очередь, может стать одним из факторов расстройств функции мембранного аппарата клеток, их ферментных систем, процессов транспорта ионов и воды, а также механизмов регуляции клетки.
 2015-05-22
2015-05-22 2261
2261
