Термодинамика устанавливает связь между ЭДС гальванического элемента и термодинамическими характеристиками токообразующей реакции.
ЭДС гальванического элемента (Е) есть разность равновесных потенциалов электродов при разомкнутой внешней цепи. Если токообразующий процесс проходит в обратимых условиях, то гальванический элемент производит максимальную работу Аmах, которая равна убыли энергии Гиббса токообразующей реакции:
Amax =-nFE =DGp=SDGкон - SDGнач,
где nF- заряд моля вещества,
Е - работа по переносу единицы заряда.
Производная Аmах по температуре может быть выражена как
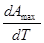 = nF
= nF 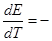
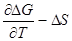 .
.
Значения же DG и DS связаны с DН уравнением Гиббса-Гельмгольца:
DН =DG + TDS, или DG=DH-TDS. Таким образом, по известным DH,DG,DS токообразующей реакции можно просто рассчитать ЭДС гальванического элемента и ее температурную зависимость.
Часто применяется и обратное решение - по величине ЭДС обратимо работающего гальванического элемента и ее температурной зависимости рассчитывают термодинамические характеристики токообразующих реакций и участвующих в них веществ.
Как правило, зависимость Е от Т прямолинейна (рис.1.10):
Е = А + В Т.
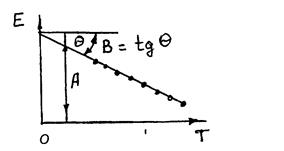
Рис.1.10. Температурная зависимость ЭДС
Умножив обе части уравнения на nF, получаем
nFE = nFA + nFBT,
-DG=-DH+DST.
Методом ЭДС получено 90% имеющейся в научной литературе информации о термодинамических свойствах неорганических веществ.
ЭДС гальванического элемента равна разности потенциалов электродов лишь для простых электрохимических систем (без диафрагмы):
(-) Me1/Me1A, Me2A/Me2(+)
В сложных системах появляется диффузионный потенциал (десятки милливольт)
jдиф = S(t+- t-) 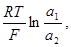
т. е., чтобы оценить величину диффузионного потенциала, надо знать t+ и t- - числа переноса катионов и анионов и активности ионов по обеим сторонам диафрагмы (a1, a2).
ЭДС гальванического элемента может быть рассчитана и как разность электродных потенциалов. Учение об электродном потенциале является основой электрохимии.
 2015-05-22
2015-05-22 3422
3422
