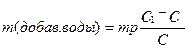 , или
, или
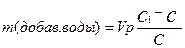 , где
, где
С1 – исходная концентрация, С – получившаяся концентрация, m – масса раствора, V – объем раствора.
Преобразованная формула нахождения концентрации C= 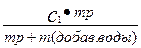
Расчет концентрации раствора при добавлении к раствору вещества.
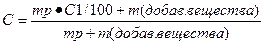
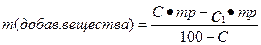
Пример:
К 327,5 г 50% – ного раствора вещества добавили 140 г воды. Массовая доля вещества в конечном растворе равна?
| Дано | Решение |
| m раствора =327,5 г W1 %=50% m (воды) = 140 г Найти: W% | 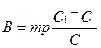 140= 140= 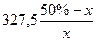 = = 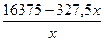 140х=16375-327,5х 140х+327,5х=16375 467,5х=16375 х=35% Ответ получившаяся концентрация 35 % Р.S. можно формулу преобразовать W% = 140х=16375-327,5х 140х+327,5х=16375 467,5х=16375 х=35% Ответ получившаяся концентрация 35 % Р.S. можно формулу преобразовать W% = 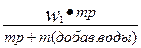 |
Реши самостоятельно:
1. К 400 г раствора, массовая доля гидроксида калия в котором 0,45, добавлено 100 г воды. Какова массовая доля щелочи в получившемся растворе?
2. В 200 г 2%-ного раствора поваренной соли растворили 20 г хлорида натрия. Какова массовая доля хлорида натрия в полученном растворе?
3. К 450 г 15 %-ного раствора гидроксида кальция добавили 60 г того же вещества. Массовая доля в конечном растворе равна?
4. Какую массу воды надо добавить к 200 г 70%-ного раствора уксусной кислоты, чтобы получить 9%-ный раствор?
5. К 300 г 10%-ного раствора сахарозы добавили 150 мл воды. Какова массовая доля сахарозы в полученном растворе?
Формулы для вычисления концентрации растворов.
| Формула | Что вычисляется по формуле | |||||||||||||
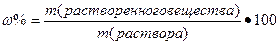 | Процентная концентрация | |||||||||||||
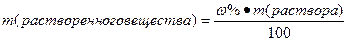 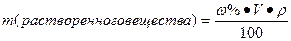 или m=Cρ10 или m=Cρ10 | Масса компонента раствора (1), масса компонента раствора в определенном объеме раствора процентной концентрации | |||||||||||||
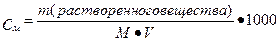 | Молярная концентрация | |||||||||||||
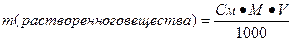 или m=CMMV или m=CMMV | Масса растворенного вещества в определенном объеме молярной концентрации | |||||||||||||
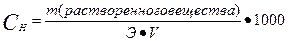 | Нормальная концентрация | |||||||||||||
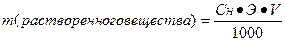 или m=CHЭV или m=CHЭV | Масса растворенного вещества в определенном объеме нормальной концентрации | |||||||||||||
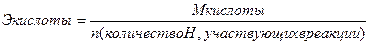 ; ; 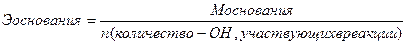 ; ; 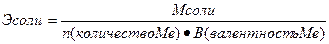 ; ; 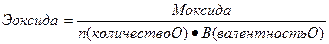 | Вычисление эквивалентов химических соединений | |||||||||||||
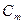 = = 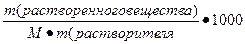 | Маляльная концентрация | |||||||||||||
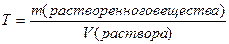 | Титр | |||||||||||||
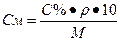 или или 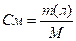 | Переход от процентной концентрации к молярной концентрации | |||||||||||||
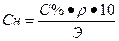 или или 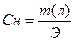 | Переход от процентной концентрации к нормальной концентрации | |||||||||||||
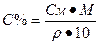 | Переход от молярной к процентной концентрации | |||||||||||||
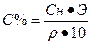 | Переход от нормальной концентрации к процентной концентрации | |||||||||||||
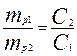 ; ; 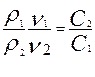 | Формулы для вычисления при приготовлении разбавленных растворов из концентрированных | |||||||||||||
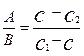 | Для вычислений при смешении растворов | |||||||||||||
 Х1 Х-Х2 Х1 Х-Х2
Х
Х2 Х1-Х Диагональная схема | Для определения отношения масс смешиваемых растворов; смешиваемого раствора и воды. | |||||||||||||
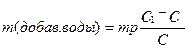 , или , или 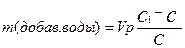 | Масса воды, которая прибавляется к раствору для разбавления его | |||||||||||||
C= 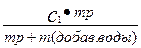 | Вычисления концентрации раствора при добавлении воды | |||||||||||||
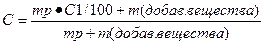 | Вычисления концентрации раствора при добавлении вещества | |||||||||||||
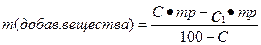 | Массы вещества, которое добавляется к раствору. |
Закрепление:
Решите задачу:
Для консервирования огурцов приготовили рассол: на 2 л воды взяли 100 г соли, а для консервирования томатов приготовили рассол из 100 г соли и 3 л воды. Какой рассол получится более концентрированным?
| Дано: V(H2O)2 = 2 л m (соли1) = 100 г V(H2O)2 = 3 л m (соли2) = 100 г ω1 -? ω2 -? | Решение: Чтобы определить массовую долю вещества в растворе воспользуемся формулой 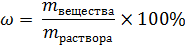 1. Найдем массу первого раствора m (р-ра1) = m (соли1) + m(H2O)1 = 100 г + 2000 г = 2100 г 2. Определим массовую долю растворенного вещества в первом растворе. 1. Найдем массу первого раствора m (р-ра1) = m (соли1) + m(H2O)1 = 100 г + 2000 г = 2100 г 2. Определим массовую долю растворенного вещества в первом растворе. 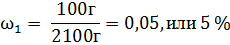 3. Найдем массу второго раствора m (р-ра2) = m (соли2) + m(H2O)2 = 100 г + 3000 г = 3100 г 4. Определим массовую долю растворенного вещества во втором растворе. 3. Найдем массу второго раствора m (р-ра2) = m (соли2) + m(H2O)2 = 100 г + 3000 г = 3100 г 4. Определим массовую долю растворенного вещества во втором растворе. 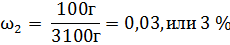 5. ω1 ˃ ω2, первый раствор более концентрированный. Ответ: рассол для консервирования огурцов более концентрированный. 5. ω1 ˃ ω2, первый раствор более концентрированный. Ответ: рассол для консервирования огурцов более концентрированный. |
 2015-06-14
2015-06-14 3189
3189


