ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ.
Живые организмы представляют собой системы с очень развитыми поверхностями раздела, к которым относятся кожные покровы, поверхность стенок кровеносных сосудов, слизистые оболочки, клеточные мембраны, мембраны ядер, митохондрий, лизосом и т.д.
Наглядное представление о значении поверхностных явлений в живом организме можно получить, рассматривая процесс дыхания, первой стадией которого является адсорбция молекул кислорода на разветвлённой поверхности альвеол лёгких. Эритроциты, обладая высокоразвитой поверхностью, адсорбируют и переносят с током крови большое количество веществ: электролитов, белков, аминокислот и других, необходимых организму. Большинство реакций, протекающих в биологических системах, совершаются при участии белков-ферментов. Первой стадией действия ферментов является адсорбция молекул субстратов на их активных центрах с образованием фермент-субстратных комплексов.
Многие жизненно важные биохимические процессы в организме протекают на поверхности биологических мембран, поэтому для понимания их механизма необходимо знание основных закономерностей, которым подчиняются поверхностные явления.
Явления, происходящие на границах раздела фаз в гетерогенных системах, называют поверхностными.
Они обусловлены особенностями состава и структуры поверхностей.
Образование поверхности раздела фаз требует совершения работы, следовательно, оно сопровождается увеличением свободной энергии системы. В поверхностном слое накапливается некоторый избыток энергии – поверхностная энергия Гиббса G S, пропорциональная площади поверхности раздела фаз S: G S = s×S.
Причиной возникновения поверхностной энергии на межфазных границах являются некомпенсированные атомные или молекулярные силы в поверхностном слое. Ненасыщенное силовое поле, возникающее на границе раздела фаз, связано с различным характером взаимодействия между молекулами в объеме и на поверхности фаз. Силы, действующие между молекулами в объеме одной фазы, называются когезионными. Силы, действующие между молекулами различных фаз, называются адгезионными.
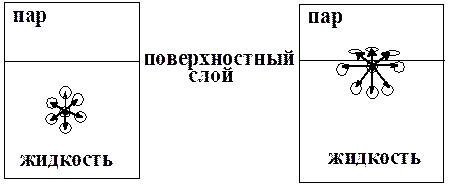 |
В объеме жидкой фазы каждая молекула находится в уравновешенном состоянии, так как силы когезионных взаимодействий со стороны таких же окружающих молекул компенсируются и результирующая (равнодействующая) сила будет равна нулю.
На молекулы, находящиеся в поверхностном слое, действуют как когезионные, так и адгезионные силы. Равнодействующая сила когезионных и адгезионных взаимодействий всегда направлена в сторону более плотной фазы и равна разности когезионных и адгезионных сил.
Равнодействующие некомпенсированные силы, действующие в поверхностном слое, являются источником свободной поверхностной энергии (G S) дисперсной гетерогенной системы.
Свободная поверхностная энергия - это термодинамическая функция, характеризующая энергию межмолекулярного взаимодействия молекул на поверхности раздела фаз с молекулами каждой из контактирующих фаз.
 GS = σ × S
GS = σ × S
где GS – свободная поверхностная энергия, Дж
S – общая поверхность раздела гетерогенной системы, м 2
σ – удельная поверхностная энергия или коэффициент поверхностного натяжения, Дж/м 2 или Н/м
Согласно второму закону термодинамики, свободная энергия системы для самопроизвольно протекающих процессов должна уменьшаться, т.е. DGS < 0,
что возможно в двух случаях:
1. при уменьшении коэффициента поверхностного натяжения,
Ds < 0, следовательно D GS = S × D s < 0;
2. при уменьшении площади общей поверхности системы,
DS < 0, следовательно D GS = s× D S < 0;
В первом случае для снижения величины s необходимо увеличить адгезионное взаимодействие, что возможно при переходе молекул третьего компонента на границу раздела фаз.
Во втором случае сокращение поверхности раздела фаз возможно за счёт объединения частиц дисперсной фазы (S 1 + S 2 > S общ .) D S < 0 Þ D GS < 0
 2015-06-14
2015-06-14 2048
2048
