1) 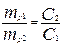 ;
;
2) 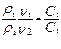
Пример:
Для получения суперфосфата применяют 65%-ный раствор серной кислоты. Сколько 92%-ного раствора серной кислоты и воды потребуется для приготовления 1 т этого раствора?
| Дано | Решение |
| С1 =65% С2 = 92% m1 =1 т Найти: массу Н2SO4 (m2), и массу Н2О | 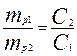 , из формулы выражает m2 , из формулы выражает m2 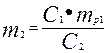 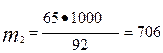 кг. m (H2O)=1000-706=294 кг Ответ: масса Н2SO4=706 кг, масса H2O=294 кг. кг. m (H2O)=1000-706=294 кг Ответ: масса Н2SO4=706 кг, масса H2O=294 кг. |
Реши самостоятельно.
1. Какие объемы 37 % раствора НСl (ρ=1,19 г/см3) и воды нужны для приготовления 1 л 10 % раствора (ρ=1,049 г/см3).
2. Какие объёмы 95% раствора серной кислоты (ρ=1835 г/л) и воды нужно для приготовления 1 л 25% раствора (ρ=1180 г/л).
3. Сколько 65% -ного раствора азотной кислоты и воды нужно взять для приготовления 500г 15%-ного раствора этой кислоты?
4. Какие объемы 30% ортофосфорной кислоты (ρ=1,18 г/см3) и воды нужны для приготовления 100 л 8% раствора (ρ=1,04 г/см3).
5. Сколько 22 н раствора плавиковой кислоты (ρ=1123 г/л) и 10 н раствора плавиковой кислоты (ρ=1036 г/л) потребуется для приготовления 20 н раствора?
 2015-06-14
2015-06-14 4061
4061
