Равновесие в процессе гидролиза солей подчиняется действующих масс закону. Если в результате гидролиза образуется нерастворимое или легколетучее вещество, гидролиз идёт практически до полного разложения исходной соли. В остальных случаях гидролиз солей проходит тем полнее, чем слабее соответствующая соли кислота или основание.
Если гидролизу подвергается соль, образованная слабой кислотой и сильным основанием, например KCN, раствор имеет щелочную реакцию; это объясняется тем, что анион слабой кислоты частично связывает образовавшиеся при диссоциации воды ионы Н+ и в растворе остаётся избыток ионов OH-:
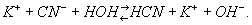
Раствор соли сильной кислоты и слабого основания, например NH4Cl, — кислый
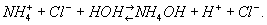
Если заряд катиона (или аниона) соли больше единицы, то гидролиз часто приводит к образованию кислых (или основных) солей в качестве продуктов первой ступени процесса, например:
CuCl2 ® Cu (OH) Cl ® Cu (OH)2.
Количественной характеристикой гидролиза солей может служить степень гидролиза (β), определяемая отношением концентрации гидролизованной части молекул к общей концентрации данной соли в растворе; в большинстве случаев она невелика. Так, в 0,1 молярных растворах ацетата натрия CH3COONa или хлорида аммония NH4CI при 25 °С β = 0,01%, а для ацетата аммония CH3COONH4 a = 0,5%. С повышением температуры и разбавлением раствора степень гидролиз увеличивается.
 2015-06-14
2015-06-14 586
586








