Легкоокисляющимися являются вещества, которые содержат функциональные группы с подвижным атомом водорода (глюкоза, аскорбиновая кислота, адреналин, викасол, производные фенотиазина и др.). Процесс окисления происходит в результате присутствия кислорода в воде и над раствором и усиливается во время тепловой стерилизации. Продукты окисления, обычно более токсичные или физиологически неактивные соединения.
Согласно теории цепных реакций процесс окисления начинается со взаимодействия свободного радикала с молекулой вещества. Свободные радикалы образуются под действием инициирующих факторов:
- световой энергии;
- тепловой энергии;
- примесей веществ, легко распадающихся на ионы и т.д.
Свободный радикал начинает цепь окислительных превращений, которую схематично можно представить следующим образом:
hv,свет 02 RН
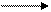
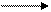
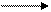
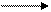 R и т.д. R . RO2 . ROOH R .
R и т.д. R . RO2 . ROOH R .
окисляемый алкильный перекисный гидроперекисный
субстрат радикал радикал радикал
Для подавления процесса окисления используют специальные вещества - антиоксиданты (восстановители, ингибиторы), которые делят на три группы:
1. Вещества, реагирующие с алкильным радикалом R*, в результате чего в R02* будет превращаться только часть R* (хиноны, нитросоединения, йод, многоядерные ароматические соединения типа антрацена). Эффективны только в условиях недостатка кислорода, поэтому в фармации не применяются.
2. Вещества, реагирующие с перекисным радикалом R02*, что снизит образование ROOH (фенолы, нафтолы, ароматические амины, аминофенолы). Данные антиоксиданты считаются наиболее эффективными ингибиторами процесса окисления.
3. Вещества, реагирующие с гидроперекисным радикалом ROOH, разрушающие гидропероксиды с образованием молекулярных продуктов (натрия сульфит и метабисульфит, тиомочевина, ронгалит, унитиол, тиомолочная кислота). Данная группа веществ так же достаточно эффективна. Стабилизирующее действие многих антиоксидантов основано на том, что они обладают большей интенсивностью окислительно-восстановительных процессов (низкий редокс-потенциал) и поэтому окисляются быстрее, чем лекарственные вещества, связывая кислород в растворе и в воздушном пространстве над ним. В качестве антиоксидантов для стабилизации легкоокисляющихся веществ могут использоваться вещества с более низким редокс-потенциалами. Например, редокс-потенциал кислоты аскорбиновой равен - 0,34, поэтому для сё стабилизации можно применять натрия сульфит, редокс-потенциал которого равен 0,19.
Комплексообразователи (отрицательные катализаторы)
Известно, что окислительно-восстановительные процессы усиливаются при попадании в инъекционный раствор даже следов тяжелых металлов с переменной валентностью (железо, медь, хром, марганец и др.), которые могут содержаться в стекле, материале аппаратуры или содержаться в качестве примесей в исходных материалах.Тяжелые металлы с переменной валентностью способны отрывать электроны от присутствующих вместе с ними в растворах различных ионов, переводя последние в радикалы:

 Сu 2+ + ROO' Сu+ + ROO . Сu 2+ + ROOH R .
Сu 2+ + ROO' Сu+ + ROO . Сu 2+ + ROOH R .
Образовавшийся радикал может реагировать с кислородом с образованием пероксидного радикала, который далее будет участвовать в цепной реакции, по приведенной ранее схеме. Частично восстановленный при этом ион тяжелого металла может легко окисляться кислородом в первоначальную форму, после чего процесс повторяется:
О2
 Сu+ Сu2+
Сu+ Сu2+
Для связывания ионов тяжелых металлов используют комплексообразователи: трилон В, тетацин-кальций, ЭДТА, производные 8- оксихинолинов. Механизм стабилизующего действия комплексонов заключается в переводе катионов тяжелых металлов в комплексные, практически недиссоциирующие соединения, неактивные по отношению к гидроперекиси. Комплексоны являются косвенными антиоксидантами.
Пути предотвращения окислении лекарственных веществ
Окилительно-восстановительное разложение лекарственных веществ зависит от множества факторов:
- наличия кислорода в воде и над раствором,
- воздействия световой энергии;
- тeмпepaтypнoгo режима;
- рН среды;
- наличия примесей тяжелых металлов и т.д.
В связи с этим стабилизация инъекционных растворов легкоокисляющихся веществ осуществляется путем использования одновременно ряда технологических приемов:
- введение антиоксидантов (мя прерывания цепной реакции окисления для связывания кислорода);
- введение раствора комплексонов или других веществ, связывающих ионы тяжелых металлов;
- создание оптимальных границ рН (поскольку ионы гидроксила также оказывают каталитическое действие на окислительно-восстановительный процесс, в растворы добавляется кислота хлороводородная или буферные смеси);
- уменьшение содержания кислорода в растворителе и в воздухе (насыщение СО2, наполнение в токе инертного газа);
- использование темной светонепроницаемой тары (для уменьшения инициирующего влияния света).
 2015-06-04
2015-06-04 2045
2045