Пусть по условию задачи в реакцию вступает 20 г алюминия. При взаимодействии с кислородом выделяется 619,85 кДж тепла (Q).
Энтальпией образования (Δ H 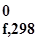 ) сложного соединения называется тепловой эффект образования 1 моля этого соединения из простых веществ, взятых в устойчивом состоянии при стандартных условиях. Единицей измерения является кДж/моль.
) сложного соединения называется тепловой эффект образования 1 моля этого соединения из простых веществ, взятых в устойчивом состоянии при стандартных условиях. Единицей измерения является кДж/моль.
Записываем уравнение химической реакции
4 Al (тв) + 3 O2 = 2 Al2O3 (тв).
Определяем количество тепла (Q) для одного моля соединения, для этого проводим сокращение и получаем
2 Al (тв) + 3/2 O2 (г) = Al2O3 (тв).
По условию задачи:
при соединении 20 г алюминия выделяется 619,85 кДж
при соединении 2-х молей алюминия, т.е. 2×27, выделяется Q кДж
Q = 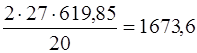 кДж.
кДж.
Так как тепло выделяется, то энтальпия системы уменьшается
Δ H 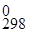 = - 1673,6 кДж/моль.
= - 1673,6 кДж/моль.
Следовательно, реакция образования оксида Al2O3 является экзотермической.
Задание 3.2. Для приведенной по варианту реакции (табл. III.2) рассчитайте: Δ H 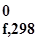 (кДж), Δ S
(кДж), Δ S 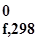 (Дж/К), Δ G
(Дж/К), Δ G 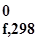 (кДж) химической реакции, вероятность ее протекания при Р = 101,3 кПа и Т = 298 К и температуру начала реакции.
(кДж) химической реакции, вероятность ее протекания при Р = 101,3 кПа и Т = 298 К и температуру начала реакции.
 2015-06-05
2015-06-05 1554
1554








