Существуют несколько эквивалентных формулировок второго начала термодинамики:
· Невозможен процесс, единственным результатом которого являлась бы передача тепла от более холодного тела к более горячему.
· Невозможен круговой процесс, единственным результатом которого было бы производство работы за счет охлаждения теплового резервуара.
· Не возможно создание вечного двигателя второго рода.
Другая формулировка второго начала термодинамики основывается на понятии энтропии:
· Энтропия изолированной системы не может уменьшаться.
Энтропия S — мера беспорядка системы, состоящей из многих элементов/
Определённая как сумма приведённых теплот, энтропия является функцией состояния и остаётся постоянной при обратимых процессах, тогда как в необратимых — её изменение всегда положительно:
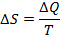
где Δ S — приращение энтропии; Δ Q — минимальная теплота, подведенная к системе; T — абсолютная температура процесса.
 2015-06-05
2015-06-05 337
337








