Федеральное агентство по образованию Российской Федерации
Филиал «Севмашвтуз» государственного образовательного учреждения высшего профессионального образования «Санкт – Петербургский государственный морской технический университет» в
Г. Северодвинске
Факультет: № 4
Кафедра: № 12
Лабораторная работа
ОПРЕДЕЛЕНИЕ ТЕПЛОЁМКОСТИ ТВЕРДЫХ ТЕЛ
Северодвинск
Лабораторная работа ФПТ 1-8
ОПРЕДЕЛЕНИЕ ТЕПЛОЁМКОСТИ ТВЕРДЫХ ТЕЛ
ЦЕЛЬ И МЕТОД РАБОТЫ
Цель работы - определение теплоемкости образцов металлов калориметрическим методом с использованием электрического нагрева.
ОСНОВНЫЕ ТЕОРЕТИЧЕСКИЕ ПОЛОЖЕНИЯ
Из теории идеального газа известно, что средняя кинетическая энергия одноатомных молекул (изолированных частиц)
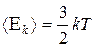
где 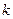 - постоянная Больцмана.
- постоянная Больцмана.
Тогда среднее значение полной энергии частицы при колебательном движении в кристаллической решетке
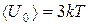
Полную внутреннюю энергию одного моля твердого тела получим, умножив среднюю энергию одной частицы, на число независимо колеблющихся частиц, содержащихся в одном моле, т.е. на постоянную Авогадро NA:
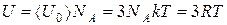 (8.1)
(8.1)
где R - универсальная газовая постоянная. R= 8,31 Дж/(мольК).
Физическая величина, определяемая отношением сообщенного системе количества теплоты к изменению температуры системы, называется теплоемкостью C системы, т. е. 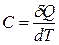
Теплоемкость измеряется в системе СИ в 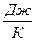 , в системе СГС в
, в системе СГС в 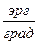 . Внесистемные единицы теплоемкости
. Внесистемные единицы теплоемкости 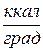 и
и 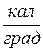 , причем, соотношения этих единиц равны:
, причем, соотношения этих единиц равны: 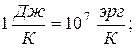
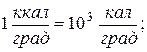
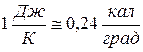 .
.
Удельной теплоемкостью вещества называется величина, равная количеству теплоты, которую необходимо сообщить единице массы вещества для увеличения ее температуры на один Кельвин: 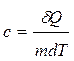
Удельная теплоемкость измеряется в 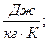
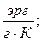
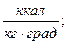 и
и 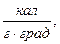 а их соотношение:
а их соотношение: 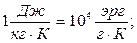
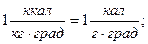
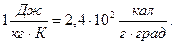
Теплоемкость одного моля вещества называется молярной теплоемкостью:
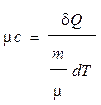
где т - масса, µ - молярная масса вещества.
Молярная теплоемкость измеряется в 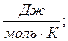
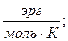
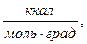 а их соотношения:
а их соотношения: 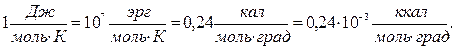
Для твердых тел вследствие малого коэффициента теплового расширения теплоемкости при постоянном давлении и постоянном объеме практически не различаются. Поэтому, учитывая (8.1) молярная теплоемкость твердого тела
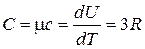 (8.2)
(8.2)
Подставляя численное значение молярной газовой постоянной, получим:
С=µс = 25 Дж/Моль К
Это равенство, называемое законом Дюлонга и Пти, выполняется с довольно хорошим приближением для многих веществ при комнатной температуре.
Со снижением температуры теплоемкости всех твердых тел уменьшаются,
приближаясь к нулю при T—»0. Вблизи абсолютного нуля молярная теплоемкость всех тел пропорциональна T3, и только при достаточно высокой, характерной для каждого вещества температуре начинает выполняться равенство (8.2). Эти особенности теплоемкостей твердых тел при низких температурах можно объяснить с помощью квантовой теории теплоемкости, созданной Эйнштейном и Дебаем.
Для экспериментального определения теплоемкости исследуемое тело помещается в калориметр, который нагревается электрическим током. Если температуру калориметра с исследуемым образцом очень медленно увеличивать от начальной Т0 на DT, то энергия электрического тока пойдет на нагревание образца и калориметра:
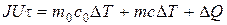 (8.3)
(8.3)
где J и U - ток и напряжение нагревателя; 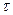 - время нагревания; т0 и т - массы калориметра и исследуемого образца, сQ и с - удельные теплоемкости калориметра и исследуемого образца, DQ - потери тепла в теплоизоляцию калориметра и в окружающее пространство.
- время нагревания; т0 и т - массы калориметра и исследуемого образца, сQ и с - удельные теплоемкости калориметра и исследуемого образца, DQ - потери тепла в теплоизоляцию калориметра и в окружающее пространство.
Для исключения из уравнения (8.3) количества теплоты, расходованной на нагрев калориметра, и потери теплоты в окружающее пространство, необходимо при той же мощности нагревателя нагреть пустой калориметр (без образца) от начальной температуры Т0 на ту же разность температур DT. Потери тепла в обоих случаях будут практически одинаковыми и очень малыми, если температура защитного кожуха калориметра в обоих случаях постоянная и равна комнатной:
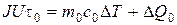 (8.4)
(8.4)
Из уравнений (8.3) и (8.4) вытекает
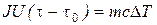 (8.5)
(8.5)
Уравнение (8.5) может быть использовано для экспериментального определения удельной теплоемкости материала исследуемого образца. Изменяя температуру калориметра, необходимо построить график зависимости разности времени нагрева от изменения температуры исследуемого образца: 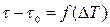 , по
, по
угловому коэффициенту 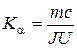 которого можно определить удельную теплоемкость образца
которого можно определить удельную теплоемкость образца 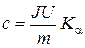 .
.
 2015-06-26
2015-06-26 577
577







