Каждое ГЛС имеет определенное внешнее оформление: этикетку, которая наклеена непосредственно на упаковку, упаковочный лист, бандероль, инструкцию, листок-вкладыш, в которых указан способ применения ГЛС.
Маркировка лекарственных средств в Украине должна соответствовать ГСТУ 64-7-2000 (Графическое оформление лекарственных средств. Общие требования).
К требованиям графического оформления упаковки относятся:
§ информационная функция упаковки должна быть обеспечена четкой и контрастной печатью, возможностью легкого считывания информации;
§ производить эстетическое влияние на потребителя;
§ иметь высокий художественный и технологический уровень обеспечения маркировки.
Текст маркировки лекарственного средства должен нести следующую информацию на украинском языке:
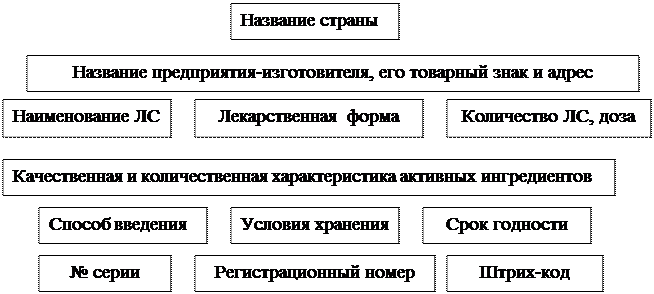
На первичной упаковке в виде блистера, первичной упаковке суппозиториев, тубе и т.п. приводится следующая информация:
 |
На первичной упаковке небольшого размера (ампулы, тюбик-капельницы, шприц-тюбика и т.п.), которая помещается во вторичную упаковку, приводятся такие данные:

Регистрационный номер лекарственных средств, зарегистрированных до августа 2003 г., содержит следующую информацию: буквы "Р" или "П" в зависимости от регистрационной процедуры означают регистрацию или перерегистрацию лекарственного средства соответственно, далее четыре цифры обозначают месяц и год регистрации, после риски пятизначное число показывает порядковый номер регистрации, который вносится в Государственный реестр лекарственных средств Украины.
| |||
| |||
|
 Согласно Приказу МЗ Украины № 358 от 29 июля 2003 г. регистрационный номер ЛС состоит из буквенного кода Украины "UA", после риски следует четыре цифры порядкового номера ЛС в Государственном реестре, затем по две цифры обозначений каждой новой лекарственной формы и каждой новой силы действия (т.е. каждой новой дозировки) конкретного ЛС. Дата регистрации и номер Приказа МЗ Украины указывается на листке-вкладыше, прилагаемом к ГЛС.
Согласно Приказу МЗ Украины № 358 от 29 июля 2003 г. регистрационный номер ЛС состоит из буквенного кода Украины "UA", после риски следует четыре цифры порядкового номера ЛС в Государственном реестре, затем по две цифры обозначений каждой новой лекарственной формы и каждой новой силы действия (т.е. каждой новой дозировки) конкретного ЛС. Дата регистрации и номер Приказа МЗ Украины указывается на листке-вкладыше, прилагаемом к ГЛС.
|
 Номер серии ЛС обозначается арабскими цифрами. Слово "серия" не указывается. Последние четыре цифры номера означают месяц и год производства ЛС, цифры перед датой указывают производственный номер серии.
Номер серии ЛС обозначается арабскими цифрами. Слово "серия" не указывается. Последние четыре цифры номера означают месяц и год производства ЛС, цифры перед датой указывают производственный номер серии.
|
Номер серии лекарственного средства должен быть указан на первичной и вторичной упаковке.
Для лекарственных средств, выработанных одним предприятием (в упаковке "ангро"), а расфасованных другим, указывается номер серии предприятия, которое фасовало лекарственное средство.
Срок годности следует указывать: "Годен до..." или (при малых размерах печатного поля) - "до...". Римскими цифрами указывается месяц, арабскими - две последние цифры года. Допускается отмечать месяц арабскими цифрами. Высота цифр должна быть не более 5 мм.
" Годен до X 2001" ("Годен до Х 2001") или "До X 2001" ("До Х 2001") - определяет пригодность до октября 2001 года;
Допускается обозначение "Годен до X 01" ("пригодный до Х 01") или "До Х 01"("До Х 01").
Для лекарственных средств, фасуемых в тубы, допускается обозначение срока годности на тубе в виде – "Срок годности 2 года".
Для лекарственных средств, в форме капель, при необходимости, следует указывать срок годности лекарственного средства после раскрытия упаковки – "Срок годности после раскрытия... суток".
На упаковке лекарственного растительного сырья необходимо дополнительно указывать требования относительно условий и срока хранения приготовленного настоя.
В случаях маркировки комплекта антибиотика с растворителем, на пачке должен быть указан номер серии антибиотика и номер серии растворителя, а также срок годности лекарственного средства (антибиотика).
Если для лекарственного средства определен ежегодный контроль по показателям качества, то на упаковке указывают "Контролируется ежегодно".
Для лекарственных средств, содержащих сильнодействующие и ядовитые вещества, на потребительской упаковке указывают надпись-предупреждение "Применять по назначению врача".
Условия хранения указываются в соответствии с требованиями, определенными разработчиком лекарственного средства.
Штриховое кодирование, печать и размещение штрих-кодовых пометок на первичной и вторичной упаковке должно быть выполнено в соответствии с требованиями Национальных стандартов Украины и руководящих нормативных документов по штриховому кодированию товарной продукции.
Адрес предприятия-производителя должен быть указан полностью. Допускается не указывать полный адрес предприятия-производителя на первичной упаковке в случаях, если этикетка первичной упаковки имеет малые размеры печатного поля и название предприятия-производителя включает в себя информацию о местонахождении предприятия.
Вторичная упаковка и этикетка групповой тары должны содержать полный адрес предприятия-производителя.
Открытое акционерное общество "Фармак", г. Киев, ул. Фрунзе, 74;
Допускается указывать:
ОАО "Фармак", г. Киев, ул. Фрунзе, 74;
ОАО "Фармак", г. Киев (при малых размерах печатного поля).
Акционерное общество "Киевмедпрепарат",
г. Киев, ул. Саксаганского, 139;
Допускается указывать:
АО "Киевмедпрепарат", г. Киев, ул. Саксаганского, 139.
АО "Киевмедпрепарат", (при малых размерах печатного поля).
Название лекарственного средства должно быть указано на латинском и украинском языках.
К каждому реализуемому лекарственному средству, прикладывается инструкция о применении, которая должна содержать:
- наименование лекарственного средства;
- общую характеристику (химическое название, основные физико-химические свойства, состав);
- сведения о фармакологических свойствах;
- показания для применения;
- противопоказания;
- взаимодействие с другими лекарственными средствами;
- способы применения и дозы;
- побочное действие;
- формы выпуска;
- условия и сроки хранения;
- условия отпуска.
 2015-06-28
2015-06-28 3155
3155