Фолдинг – это процесс укладки вытянутой полипептидной цепи в правильную трехмерную пространственную структуру. Для обеспечения фолдинга используется группа вспомогательных белков под названием шапероны (chaperon, франц. – спутник, нянька). Они предотвращают взаимодействие новосинтезированных белков друг с другом, изолируют гидрофобные участки белков от цитоплазмы и "убирают" их внутрь молекулы, правильно располагают белковые домены. Шапероны представлены семействами, состоящими из гомологичных по строению и функциям белков, которые отличаются по характеру экспрессии и присутствию в разных компартментах клетки.
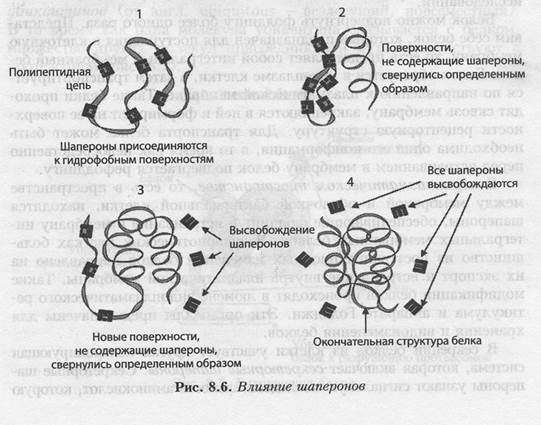
В целом шапероны способствуют переходу структуры белков от первичного уровня до третичного и четвертичного, но они не входят в состав конечной белковой структуры.
Новосинтезированные белки после выхода с рибосом для правильного функционирования должны укладываться в стабильные трехмерные структуры и оставаться такими на протяжении всей функциональной жизни клетки. Поддержание контроля качества структуры белка и осуществляется шаперонами, катализирующими укладку полипептидов. Сборка полипротеинов и укладка мультибелковых комплексов также осуществляется шаперонами. Шапероны связываются с гидрофобными участками неправильно уложенных белков, помогают им свернуться и достигнуть стабильной нативной структуры и, тем самым, предотвращают их включение в нерастворимые и нефункциональные агрегаты. В течение своей функциональной жизни белок может подвергаться различным стрессам и денатурации. Такие частично денатурированные белки могут стать, во-первых, мишенью протеаз, во-вторых, агрегировать и, в-третьих, укладываться в нативную структуру с помощью шаперонов. Баланс и эффективность, с которой происходят эти три процесса, определяются соотношением компонентов, участвующих в этих реакциях.
- Транспорт многих белков из одного компартмента в другой.
- Участие в сигнальных путях. Например, присутствие Hsp70 необходимо для активации фосфатазы, которая путем дефосфорилирования ингибирует протеинкиназу JNK, компонент сигнала стресс-индуцированного апоптоза, т.е. Hsp70 является частью антиапоптозного сигнального пути.
- Регуляция функций различных молекул. Например, стероидный рецептор, находящийся в цитоплазме, связан с Hsp90; лиганд, попадающий в цитоплазму, присоединяется к рецептору и вытесняет шаперон из комплекса. После этого комплекс рецептор-лиганд приобретает способность связываться с ДНК, мигрирует в ядро и осуществляет функцию транскрипционного фактора.
При нарушении функции шаперонов и отсутствии фолдинга в клетке формируются белковые отложения – развивается амилоидоз. Амилоид представляет собой гликопротеид, основным компонентом которого являются фибриллярные белки. Они образуют фибриллы, имеющие характерную улырамикроскопическую структуру. Фибриллярные белки амилоида неоднородны. Насчитывают около 15 вариантов амилоидоза.
Прио́ны
Складывается впечатление, что фолдинг с участием фолдаз и шаперонов приводит к правильной. Наиболее оптимальной в энергетическом и функциональном отношениях структкре. Однако это не так. Существует группа тяжелых неврологических болезней, обусловленных неправильным фолдингом одного, вполне определенного белка.
Известно, что PrP может существовать в двух конформациях — «здоровой» — PrPC, которую он имеет в нормальных клетках (C — от англ. cellular — «клеточный»), в которой преобладают альфа-спирали, и «патологической» — PrPSc, собственно прионной (Sc- от scrapie), для которой характерно наличие большого количества бета-тяжей.
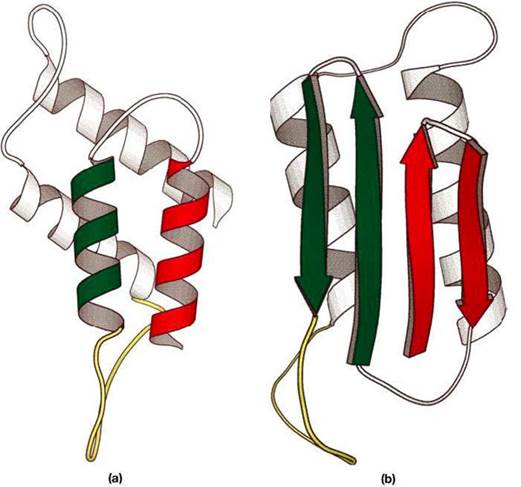
Прионный белок, обладающий аномальной трёхмерной структурой, способен прямо катализировать структурное превращение гомологичного ему нормального клеточного белка в себе подобный (прионный), присоединяясь к белку-мишени и изменяя его конформацию. Как правило, прионное состояние белка характеризуется переходом α-спиралей белка в β-слои.
При попадании в здоровую клетку, PrPSc катализирует переход клеточного PrPC в прионную конформацию. Накопление прионного белка сопровождается его агрегацией, образованием высокоупорядоченных фибрил (амилоидов), что в конце концов приводит к гибели клетки. Высвободившийся прион, по-видимому, оказывается способен проникать в соседние клетки, также вызывая их гибель.
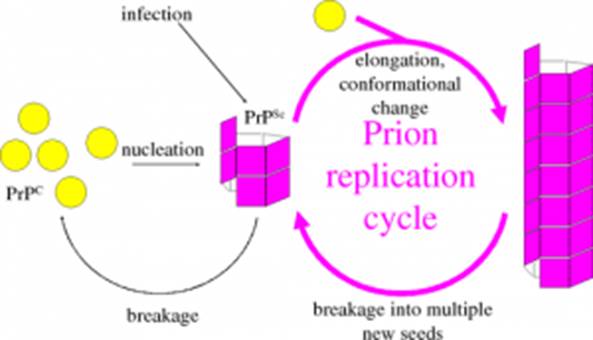
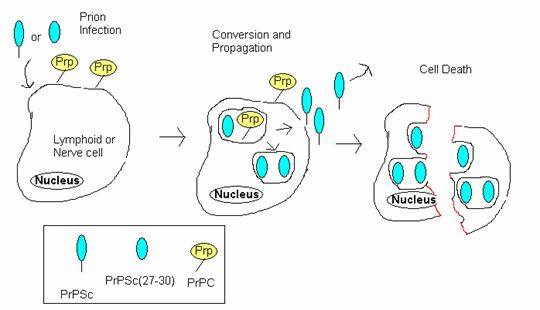
Функции белка PrPC в здоровой клетке — поддержание качества миелиновой оболочки, которая в отсутствие этого белка постепенно истончается. В норме белок PrPC ассоциирован с клеточной мембраной, гликозилирован остатком сиаловой кислоты. Он может совершать циклические переходы внутрь клетки и обратно на поверхность в ходе эндо- и экзоцитоза.
До конца механизм спонтанного возникновения прионных инфекций не ясен. Считается (но ещё не полностью доказано), что прионы образуются в результате ошибок в биосинтезе белков. Мутации генов, кодирующих прионный белок (PrP), ошибки трансляции, процессы протеолиза — считаются главными кандидатами на механизм возникновения прионов.
Таким образом, прио́ны — особый класс инфекционных агентов, чисто белковых, не содержащих нуклеиновых кислот, вызывающих тяжёлые заболевания центральной нервной системы у человека и ряда высших животных (т. н. «медленные инфекции»).
Есть данные, дающие основание считать, что прионы являются не только инфекционными агентами, но и имеют функции в нормальных биопроцессах. Так, например, существует гипотеза, что через прионы осуществляется механизм генетически обусловленного стохастического старения.
Прионы — единственные известные инфекционные агенты, размножение которых происходит без участия нуклеиновых кислот.
Во второй половине XX века врачи столкнулись с необычным заболеванием человека — постепенно прогрессирующим разрушением головного мозга, происходящим в результате гибели нервных клеток. Это заболевание получило название губчатой энцефалопатии. Похожие симптомы были известны давно, но наблюдались они не у человека, а у животных (скрейпи овец), и долгое время между ними не находили достаточной обоснованной связи.
Новый интерес к их изучению возник в 1996 г., когда в Великобритании появилась новая форма заболевания, обозначаемая как «новый вариант болезни Крейтцфельдта-Якоба.
Важным событием было распространение «коровьего бешенства» в Великобритании, эпидемия которого была сначала в 1992—1993 гг, а потом и в 2001 г охватила несколько европейских государств, но тем не менее экспорт мяса во многие страны не был прекращён. Заболевание связывают с использованием «прионизированной» костной муки в кормах и премиксах, изготовленной из туш павших или заболевших животных, возможно, и не имевших явных признаков заболевания.
Пути переноса причинного фактора болезни, механизмы проникновения прионов в организм и патогенез заболевания изучены пока недостаточно.
Прионы млекопитающих — возбудители губчатой энцефалопатии
Скрейпи овцы и козы Прион скрейпи OvPrPSc
Трансмиссивная энцефаломиопатия норок (ТЭН) Прион ТЭН и MkPrPSc
Chronic wasting disease (CWD) олени и лоси CWD прион MDePrPSc
Губчатая энцефалопатия крупного рогатого скота (ГЭКРС) Коровы Прион ГЭКРС BovPrPSc
Губчатая энцефалопатия кошачьих (ГЭК) Кошки Прион ГЭК FePrPSc
Губчатая энцефалопатия экзотических копытных (EUE) Антилопы и большой куду EUE прион NyaPrPSc
Куру Люди Прион куру HuPrPSc
Болезнь Крейцфельда-Якоба (БКЯ) Люди Прион БКЯ HuPrPSc
(New) Variant Creutzfeldt-Jakob disease (vCJD, nvCJD) Люди vCJD прион HuPrPSc
Синдром Герстманна—Штройслера—Шейнкера (GSS) Люди GSS прион HuPrPSc
Фатальная семейная бессонница (ФСБ) Люди Прион ФСБ HuPrPS
Человек может заразиться прионами, содержащимися в пище, так как они не разрушаются ферментами пищеварительного тракта. Так как стенками кишечника они не адсорбируются, то могут проникать в кровь только через поврежденные ткани. В конечном итоге они попадают в центральную нервную систему. Так переносится новый вариант болезни Крейтцфельдта-Якоба (nvCJD), которой люди заражаются после употребления в пищу говядины, содержащей нервную ткань из голов скота, больных бычьей губчатой энцефалопатией (BSE, коровье бешенство).
На практике доказана возможность прионов заражать организм мышей воздушно-капельным путем.
Прионы могут проникать в тело и парентеральным путем. Были описаны случаи заражения при внутримышечном введении препаратов, изготовленных из человеческих гипофизов (главным образом гормоны роста для лечения карликовости), а также заражение мозга инструментами при нейрохирургических операциях, поскольку прионы устойчивы к применяемым в настоящее время термическим и химическим методам стерилизации. Эта форма болезни Крейтцфельдта-Якоба обозначается как ятрогенная (1CJD).
При определённых, неизвестных условиях, в организме человека может произойти спонтанная трансформация прионного белка в прион. Так возникает так называемая спорадическая болезнь Крейтцфельдта-Якоба (sCJD), впервые описанная в 1920 г. независимо друг от друга Гансом Герхардом Крейтцфельдтом и Альфонсом Марией Якобом. Предполагается, что спонтанное возникновение этой болезни связано с фактом, что в норме в человеческом теле постоянно возникает небольшое количество прионов, которые эффективно ликвидируются клеточным Аппаратом Гольджи. Нарушение этой способности «самоочищения» клеток может привести к повышению уровня прионов выше допустимой границы нормы и к их дальнейшему неконтролируемому распространению. Причиной возникновения спорадической болезни Крейтцфельдта-Якоба согласно этой теории является нарушение функции Аппарата Гольджи в клетках.
Особую группу прионовых заболеваний представляют собой наследственные (врожденные) болезни, вызванные мутацией гена прионового белка, который делает возникший прионовый белок более подверженным спонтанному изменению пространственной конфигурации и превращения их в прионы. К этой группе наследственных заболеваний относится и наследственная форма болезни Крейтцфельдта-Якоба (fCJD), которая наблюдается в ряде стран мира. При прионовой патологии наивысшая концентрация прионов обнаружена в нервной ткани заражённых людей. Прионы встречаются в лимфатической ткани. Наличие прионов в биологических жидкостях, включая слюну, пока не было однозначно подтверждено. Если представление о постоянном возникновении небольшого количества прионов верно, то можно предположить, что новые, более чувствительные методы диагностики откроют это количество прионов, разбросанное по различным тканям. В данном случае, однако, речь пойдёт о «физиологическом» уровне прионов, которые не представляют собой никакой угрозы для человека.
 2015-06-28
2015-06-28 17132
17132








