То, что гены расположены в хромосомах, казалось бы, не соответствует тому факту, что у людей только 23 пары хромосом и вместе с тем тысячи различных признаков, которым должны соответствовать тысячи различных генов. Одних только признаков, сцепленных с Х-хромосомой, несколько сотен, а на самой короткой аутосоме расположены также сотни генов. Как это согласуется с менделевским законом независимого распределения признаков? Это значит, что закон независимого распределения признаков применим только для генов, расположенных на разных хромосомах; сначала ученым необходимо было определить основные законы и выяснить природу наследственности на примере простейших признаков. На самом деле многие гены расположены на одной и той же хромосоме, поэтому они, как правило, наследуются вместе. Такие гены называются сцепленными. Одно из достижений современной генетики и заключается в том, что созданы карты сцепления для многих признаков. На этих картах показано также относительное положение генов на хромосомах, и мы увидим, что эти карты имеют не только теоретическое, но и практическое значение.
Место, которое ген занимает на хромосоме, называется локусом. За исключением тех редких случаев, когда происходит перестройка хромосомы, у всех представителей отдельного биологического вида каждый ген имеет строго определенный локус. Мы уже говорили, что о существовании генов узнали по мутациям, которые обычно изменяют гены, делая их дефектными или необычными. Большинство наследственных признаков известны по таким наследственным заболеваниям, как гемофилия, дальтонизм и фенилкетонурия. Нормальные аллели гена называются дикими, хотя, как правило, этот термин применим только для некоторых организмов, с которыми проводят опыты. Гены, определяющие такие признаки человека, как цвет глаз или группу крови, обычно дикими не называются. В естественной популяции имеется много аллелей одного гена. Мутантный аллель можно использовать как маркер, помогающий определить местоположение гена. Например, дефектный ген гемоглобина, который вызывает серповидноклеточную анемию, можно использовать как маркер для определения локуса генов гемоглобина вообще. Без такого варианта гена у нас бы было мало возможностей исследовать эти гены.
Генетическая карта хромосомы представляет собой линию, на которой отмечены локусы генов и относительные расстояния между ними, измеряемые в единицах карты. Хотя некоторые методы с использованием микроскопа позволяют ученым непосредственно определить локус гена на хромосоме, обычно устанавливают локус гена относительно других генов. Для этого требуются организмы, гетерозиготные по двум генам, чтобы две маркированные хромосомы могли взаимодействовать друг с другом. Распределение аллелей в этих организмах называется родительской комбинацией. Гены обозначаются буквами на двух линиях хромосом, иногда схему упрощают до одной линии:

Маркеры, обозначенные буквами сверху, располагаются на одной гомологичной хромосоме, а обозначенные буквами снизу — на другой гомологичной хромосоме. Для удобства при печати линии могут обозначаться косыми чертами, например ЛВ/аb. Поясним принцип составления карт на конкретном примере. Допустим, два гена — ген дальтонизма и гемофилии — располагаются на Х-хромосо-ме: с — аллель дальтонизма, С — аллель нормального зрения, h — аллель гемофилии, Н — аллель нормального свертывания крови. Поскольку мы не можем скрещивать людей по своему выбору, нужно собрать данные о тех семьях, в которых жены были гетерозиготны по обоим генам. Маркеры могут находиться в состоянии сопряжения, когда доминантные аллели располагаются на одной хромосоме, а рецессивные — на другой, или же в состоянии отталкивания, когда на каждой хромосоме располагаются доминантный и рецессивный аллели. Для начала рассмотрим случай, когда женщины переносят аллели в состоянии отталкивания, С h/c H. Это значит, что у них на одной Х-хромосоме аллели С и h, а на другой — с и Н. Так как сыновья получают Х-хромосому только от матери, фенотип сыновей сразу же указывает, какую хромосому они унаследовали. В данном случае можно ожидать, что половина сыновей получит ген дальтонизма, но без гена гемофилии (Н с/У), а другая половина — ген гемофилии, но без гена дальтонизма (h C/Y). В действительности же наблюдается следующее распределение:
9 С h/Y: 1 С H/Y: 1 с h/Y: 9 с H/Y.
Получается, что 10% сыновей, которых мы называем рекомбинантами, получили иную комбинацию генов, отличающуюся от комбинации их матерей.
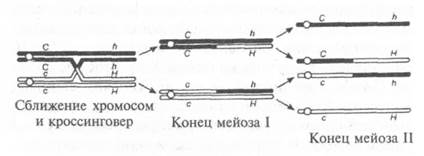
В профазе мейоза гомологичные пары выстраиваются напротив друг друга и удерживаются вместе в хиазмах, то есть в точках, где их хроматиды переплетаются друг с другом. Иногда в точке хиазмы хроматиды разрываются и обмениваются друг с другом сегментами. Такой процесс называется кроссин-говером. Если кроссинговер происходит между локусами двух генов, то аллели этих генов перераспределяются между хромосомами.
Кроссинговер приводит к рекомбинации, и число R, равное отношению числа рекомбинантов к общему числу потомков, называется частотой рекомбинации. Данные гены рекомбинируют с частотой 10% (два рекомбинанта из 20), то есть R — 0,1.
Так как рекомбинация происходит случайным образом, R зависит от вероятности того, что кроссинговер произойдет между двумя генами. Если это расстояние очень короткое, то вероятность рекомбинации будет крайне низка, и два аллеля, скорее всего, останутся на одной хромосоме. Если расстояние между генами большое, то вероятность того, что кроссинговер произойдет в точке, расположенной между ними, повышается и как следствие повышается частота рекомбинации. Таким образом, число R можно принимать за меру расстояния между двумя генами на одной хромосоме. За единицу карты условно принимают 1% рекомбинаций, поэтому, если частота рекомбинации между С и Я равна 10%, то расстояние между этими генами равно 10 единицам. Можно доказать, что частота рекомбинации определяется только расстоянием между генами, а не начальным распределением аллелей на другом примере, где аллели находятся в состоянии сопряжения. Для такого случая имеем следующие данные:
9 С H/Y: 1 С h/Y: 1 с H/Y: 9 с h/Y.
Этого и следовало ожидать: 90% начального расположения аллелей и 10% рекомбинаций.
Определить расстояние между генами человека — достаточно сложно. У большинства организмов, скрещивать которые можно по выбору, весь процесс состоит из двух стадий. Сначала скрещиваются между собой гомозиготы с нужными аллелями и получается гетерозиготное потомство, у которого могут происходить рекомбинации; затем скрещиваются особи второго поколения, и изучается их потомство. У людей первая и вторая стадии соответствуют браку, над которым мы не властны, и поэтому остается только изучать потомков от таких браков.
Установив расстояние между двумя генами, можно по одному добавлять и другие гены. Возьмем для примера ген, маркированный по аллелям Аи а и сцепленный с геном С. Исследуем распределение аллелей у сыновей от женщин с генотипом А с/а С:
43 A c/Y, 7 A C/Y, 8 a c/Y, 42 a C/Y.
Всего получается 15 (7 + 8) рекомбинаций из сотни, то есть 15%. Поэтому ген А можно поместить на хромосомной карте в 15 единицах от гена С. Однако три гена могут располагаться в последовательности Н С А, и в таком случае расстояние между A и H будет равно 25 (10 + 15) единицам, либо они могут располагаться в последовательности А Н С, и в таком случае А и H будут находиться всего в 5 (15 — 10) единицах друг от друга. Для уточнения положения третьего гена следует учесть данные скрещиваний по генам А и Н.
Легче всего определять положение генов, сцепленных с полом, потому что расположение аллелей как минимум одной из Х-хромосом женщины можно определить по Х-хромосоме ее отца, а генотип Х-хромосомы ее сыновей также определяется непосредственно. Построить карту аутосомных хромосом труднее. В наше время созданы превосходные карты для некоторых лабораторных и культурных растений и животных (рис. 8.1), но определить точный генотип человека или хотя бы расположение аллелей (сопряжение или отталкивание) нелегко.
Карты сцепления хромосом человека оказали бы неоценимую помощь генетическому консультанту. Например, одной аутосомной доминантной мутацией Ht вызывается наследственное заболевание — хорея Гентингтона. Для этого заболевания характерно ослабление со временем функционирования нервной системы, особенно после среднего возраста. Если человек болен хореей Гентингтона, то вероятность передать своему ребенку аллель Ht составляет 50%. Можно ли уменьшить вероятность?
Предположим, что существует другой ген с двумя аллелями А и а, расположенный в 5 единицах от Ht, и что определить аллели у каждого человека легко. Допустим, у больного отца будущего ребенка Генотип A Ht/a ht, а у нормальной матери генотип ht a/ht а

Рис. 8.1. Генетическая карта плодовой мушки Drosophila melanogaster
. На основании этих данных можно уточнить вероятность передачи дефектного гена. Ребенок, гомозиготный по а, с вероятностью в 95% не будет иметь Ht, потому что Ht у больного родителя связан с А и может отделиться лишь в 5% случаев. Точно так же и для ребенка с аллелем А существует вероятность 95%, что он унаследует Ht. Конечно, родителям было бы полезно узнать, переносят ли они еще не проявивший себя аллель Ht и с какой вероятностью передадут его своим детям.
Но здесь мы опять подходим к неизбежному вопросу, какую ценность имеет знание, что человек переносит ген, способный вызвать умственную отсталость у его детей или даже послужить причиной их ранней смерти. Многие предпочли бы не знать этого и в свободном обществе они имеют полное на то право. (Право на незнание стали рассматривать в недавнее время, в связи с развитием современной науки.) Однако некоторые люди были бы этому рады; такое знание избавило бы их от пугающей неопределенности и помогло бы оценить шансы завести здоровое потомство. Кроме того, медицина постоянно развивается, и появляются новые методы лечения наследственных нарушений, которые могут проявиться в более позднем возрасте, так что со временем ценность знания, что человек является переносчиком того или иного аллеля, будет только повышаться.
Аллель, который мы обозначили как а, мог быть либо геном с определенной функцией, выражаемой фенотипически, либо участком нейтральной вариации ДНК, таким, как полиморфизм длины рестрикционных фрагментов (см. далее). В обоих случаях фрагменты ДНК помогают определить наличие дефектного аллеля, но нейтральные участки встречаются чаще и потому они, как правило, более полезны.
 2015-06-28
2015-06-28 1861
1861








