Скорость химической реакции определяется энергией активации (Еакт). Энергией активации называется количество энергии в кдж, необходимое для того, чтобы все молекулы 1 моля вещества при определенной температуре достигли переходного состояния, соответствующего вершине энергетического барьера. В этой точке существует равная вероятность того, что достигшие ее молекулы вступят в реакцию с образованием продукта (Р) или вернутся обратно на уровень непрореагировавших молекул (S). Ч ем меньше энергия активации, тем легче (скорее) протекает реакция.
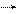 В присутствии фермента (Е) реакция (S Р) делится на несколько стадий.
В присутствии фермента (Е) реакция (S Р) делится на несколько стадий.
1 2


 S + E ES E + P
S + E ES E + P
Вначале фермент (Е) взаимодействует с субстратом (S) с образованием фермент-субстратного комплекса (ЕS). Энергия активации этой стадии невелика, и комплекс образуется быстро.
На второй стадии происходит образование продукта (Р). Поскольку энергия ES-комплекса уже достаточно высока, то энергия активации второй стадии будет опять невелика и переходное состояние ES достигается быстро.
Этот механизм обеспечивается следующими факторами:
- сближение и ориентация реакционного центра субстрата под каталитическую группу фермента;
- напряжение и деформация как субстрата, так и фермента, приводящее к увеличению энергии фермент-субстратного комплекса, что делает невыгодным его существование;
- кислотно-основный или ковалентный катализ.
 2015-06-26
2015-06-26 274
274








