1. Выразить константу равновесия химической реакции (К)
2(FeО) + [Si] = 2[Fe](чист.)+ (SiO2), приняв расплав идеальным.
2. Рассчитать константу равновесия при Т = 2200К, исходя из термодинамических величин.
3. Будет ли окисляться кремний при T = 2200K, если в металле [%Si] = 2; в шлаке (% FeO) = 10, (% SiO2) = 30?
4. В каком направлении сместится равновесие при уменьшении давления?
Задание 9
1.Выразить константу равновесия химической реакции (К)
2H2S (газ)+ 3O2(газ)= 2H2O (газ)+ 2SO2(газ)
2.Вычислить 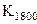 , используя расчеты
, используя расчеты 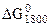 .
.
3.Возможна ли данная реакция при Т = 1800К, если {%SO2}(факт.)= 11,5; 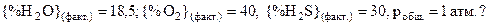
4. В каком направлении сместится равновесие химической реакции с увеличением давления?
Задание 10
1. Выразить константу равновесия химической реакции (К)
2CaF2(чист.)+ SiO2(чист.)= 2СаО (чист.)+ SiF4 (г)
2. Рассчитать константу равновесия при Т = 2000К, используя термодинамические данные.
3. Будет ли выделяться фтористый кремний SiF4в атмосферу, при Т = 2000К и 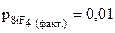 атм?
атм?
4. При каком давлении фторида кремния реакция прекратится?
 2015-07-03
2015-07-03 498
498








