ЕЛЕКТРОННА ПОЛЯРИЗАЦIЯ. Розглянемо поляризацiю неполярних молекул. Електрони рiвномiрно розподiленi навколо атомного ядра та атом не має результуючого дипольного моменту, тому поляризацiя вiдсутня. В електричному полi електрони та ядра змiщуються в протилежних напрямках (рис.5.5, а) та в результатi виникае дипольний момент.
Якщо атом елемента з атомним номером Z і радiусом R (визначається як радiус “твердої кульки”) вмiщений в електричне поле E та якщо заряд електронiв рiвномiро розподiлений по всiй сферi,то змiщення зарядiв можна представити у вiдповiдностi зi схемою зображеною на рис.5.5,б.

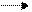

 d
d



 R
R

 R R
R R

+ -
 E
E
(а) (б)
Рис.5.5. Схема зміщення заряду електронів
На ядро атома дiє двi сили: а) cила Fп зi сторони електричного поля; б) кулонiвська сила Fк, напрямлена до центру електронної хмари, яку можна обчислити, знаючи електронний заряд у серединi пунктирного кола на рис.5.5,б.
 Fк = (-1/(4×p×eо)) [(Z2×e2×d3/R3)/d2].
Fк = (-1/(4×p×eо)) [(Z2×e2×d3/R3)/d2].
Так-як: Fп = Z×e×E = - Fк, то:
d = [4×p×eо×R3/(Ze)]×E,
де 4×p×eо×R = aел – поляризованiсть.
pел = Z×e×d = Z×e×[4×p×eо×R3/(Ze)]×E = aел×E,
Рел = N×aел×E,
де N- число атомiв в одиницi об’єму.
Висновки:
а) бiльшi атоми володiють бiльшою поляризуємiстю;
б) данi про електронну поляризуємість дозволяють оцiнити радiуси атомiв;
в) поляризуємість не залежить вiд температури.
IОННА ПОЛЯРИЗАЦIЯ. Iонна поляризацiя, як i електронна не залежить вiд температури. Характерна для твердих тiл з iонною будовою.
 2015-07-03
2015-07-03 274
274








