Общие
1.Составьте глоссарий по изучаемой теме. Включите в него следующие и другие (самостоятельно подобранные по данной теме) термины: физическая модель идеального газа, параметры состояния идеального газа, хаотическое движение молекул газа. (ОК-1, ПК- 19)
2.Изучите и запомните следующие формулы (ПК-1, ПК-19)
| Наименование величины или физический закон | Формула |
| Уравнение Менделеева – Клапейрона p – давление газа, Н/м2 , V – объем газа, м3, М – масса газа, кг, R =8,31 Дж/мольК, μ – масса одного моля газа (молярная масса) кг/моль, Т – абсолютная температура газа, К. | 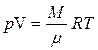
|
| Зависимость давления газа от его абсолютной температуры и от концентрации его молекул | p= nkT |
| Концентрация молекул | n = 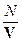
|
| Число молекул газа | N = M/m = NaM / μ |
| Постоянная Больцмана | k = 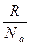 = 1,38 . 10-23 Дж/К. = 1,38 . 10-23 Дж/К.
|
3.Разберите самостоятельно следующие задачи (ОК-1, ПК-1, ПК- 3, ПК-19)
Задача 1
Определить молярную массу смеси mсм кислорода массой m1=25 г и азота массой m2=75 г.
Решение. Молярная масса mсм смеси, это отношение массы смеси mсм к количеству вещества nсм смеси:
mсм=mсм/nсм.
Масса смеси равна сумме масс компонентов смеси:
mсм=m1+m2.
Количество вещества смеси равно сумме количеств вещества компонентов
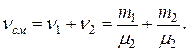
Подставив выражения mсм и nсм в ранее записанную формулу для молярной массы получим
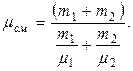
где m1=32×10-3 кг/моль, m2=28×10-3 кг/моль.
Подставив значение величин и произведя вычисление, будем иметь mсм=28,9.10-3 кг/моль.
Ответ: mсм=28,9·10-3 кг/моль.
Задача 2
Определить число молекул N, содержащихся в объеме V=1 мм3 воды, и массу m1 одной молекулы воды. Считая условно, что молекулы воды имеют вид шариков, соприкасающихся друг с другом, найти диаметр d молекул.
Решение. Число молекул N, содержащихся в некоторой системе массой m, равно произведению постоянной Авогадро на количество вещества
N=nNА.
Так как n=m/m, где – молярная масса, то
N=(m/n)NА.
 2015-07-03
2015-07-03 450
450








