Ожирение - избыточное накопление жира в организме, приводящее к увеличению массы тела на 20% и более от средних нормальных величин ("идеальная масса тела"). В настоящее время по данным ВОЗ ожирение представляет собой одно из самых распространенных заболеваний, которым в экономически развитых странах страдают до 30% населения.
Общепринятой классификации форм ожирения до сих пор нет. Различают первичную форму или алиментарно–экзогенную (до 75% общего числа страдающих ожирением), о которой говорят в тех случаях, когда без явного основного заболевания имеет место превышение нормальной массы тела. Вторичные формы ожирения могут быть обусловлены нарушениями функций эндокринных желез и церебральными нарушениями. Д.Я.Шурыгин и др. (1980) конкретизировали формы первичного и вторичного ожирения и предложили следующую классификацию:
I. Формы первичного ожирения.
1. Алиментарно-конституциональное ожирение.
2. Нейроэндокринное ожирение:
a) гипоталамо-гипофизарное ожирение;
b) адипозогенитальная дистрофия (у детей и подростков),
II. Формы вторичного (симптоматического) ожирения.
1. Церебральное.
2. Эндокринные:
a) гипотироидное;
b) гипоовариальное;
c) так называемое климактерическое;
d) надпочечниковое.
Степени ожирения: I - фактическая масса тела превышает "идеальную" не более чем на 29%; II - на 30-49%, III - на 50-99; IV - на 100% и более.
Этиология ожирения определяется многими факторами. Причины, указанные ниже, лежат в основе патогенетических механизмов развития алиментарно-экзогенного ожирения. Вместе с тем действие этих же факторов, как правило, имеет место при вторичных формах ожирения и существенно усугубляет их течение.
Ведущим фактором в развитии ожирения является положительный энергетический баланс - преобладание энергопотребления над энергозатратами, т.е. любое ожирение представляет собой в конце концов проблему баланса. При этом следует подчеркнуть, что доминирующим регулятором массы тела является поступление калорий. Общепринято считать, что ожирение является результатом переедания. Для тучных лиц характерно своеобразное пищевое "поведение" - они с удовольствием едят любую пищу. Несомненно, что недостаточная физическая активность, гиподинамия способствуют развитию ожирения, но не играют главенствующей роли.
Помимо вышеперечисленных факторов к тучности ведет несбалансированный рацион питания: потребление высококалорийной пищи с избытком жиров и легкоусвояемых углеводов. Не последнее место занимает нарушение ритма питания; питание о преобладанием потребления большей части суточного рациона в вечерние часы; редкие, но обильные приема пищи, злоупотребление специями, соленой пищей и т.д.
Конституциональный фактор, наследственная предрасположенность, в основе которых может лежать генетически обусловленная скорость метаболических реакций, также входят в число факторов, способствующих ожирению. Отмечено, что в случае ожирения у одного из родителей тучность у детей наблюдается в 40% случаев. Если ожирением страдают оба родителя, тучность у детей встречается в 80% случаев.
Доказательством, указывающими на передачу ожирения по наследству, являются наследственные синдромы, сопровождающиеся ожирением, например, синдром Лоуренса-Муна-Барде-Бидля; существование линий мышей с передающимся по наследству ожирением (линии ob/ob, db/db); высокая корреляция по массе тела у монозиготных близнецов по сравнению о дизиготными. Более непосредственных доказательств передачи ожирения по наследству у людей не обнаружено. Следует помнить, что семейный характер ожирения нередко является отражением привычек и наклонностей.
В развитии ожирения имеют значение три основных патогенетических фактора: повышенное поступление пищи, несоответствующее энергозатратам, недостаточная мобилизация жира из депо; избыточное образование жира из углеводов (С.Н.Лейтес).
Кроме того, в настоящее время в патогенезе ожирения учитывается значение особенностей самой жировой ткани, количество и величина жировых клеток. Регуляция количества жиров в организме может осуществляться путем увеличения размеров адипоцитов (гипертрофия) или путем увеличения их количества (гиперплазия). Соответственно этим двум механизмам можно разделить ожирение на гипертрофическое и пигерпластическое. Наряду с указанными существует смешанный тип ожирения (гиперпластически-гипертрофический). Изменения величины и количества адипоцитов связаны с их чувствительностью к действию регулирующих факторов, в частности некоторых гормонов. Показано, что увеличенные в размерах адипоциты обладают сниженной чувствительностью к тормозящему липолиз действию инсулина.
Для развития ожирения необходима перестройка функций организма, поддерживающих постоянную массу тела, т.е. изменение скорости и направленности обменных процессов, в регуляции которых основное место принадлежит нервной и эндокринной системам.
Регуляция аппетита - сложный многокомпонентный механизм, – одним из важных звеньев которого являются центры насыщения и голода, располагающиеся в гипоталамусе. Центр насыщения локализуется в вентромедиалных ядрах гипоталамуса, его разрушение приводит к гиперфагии. Разрушение венролатеральных ядер гипоталамуса ("центр голода") вызывает анорексию. Этот механизм регуляции аппетита называют "аппестатом".
Очевидно, при ожирении гиперфагия обусловлена запоздалыми реакциями центра насыщения, в норме тормозящего центр голода. Возможно, что наследственный дефект, обусловливающий дисфункцию центров насыщения и голода, связан с нарушением синтеза нейротрансмиттеров (моноаминов и пептидов). "Центр голода" имеет многочисленные связи с дофаминергической, тогда как "центр сытости" - с норадренергической системой. Кроме того, показано, что в регуляции поступления и расходования энергии в организме участвуют эндорфинергическая и серотонинергическая иннервация.
Основная роль в регуляции чувства сытости отводится холецистокинину. Считают, что прием пищи вызывает высвобождение холецистокинина, который снижает аппетит через афферентные окончания блуждающего нерва, расположенные в кишечнике. При ожирении снижается содержание холецистокинина в гипоталамусе, чем объясняется недостаточное угнетение чувства голода и как результат этого избыточный прием пищи.
На центры насыщения и голода могут оказывать непосредственное влияние и некоторые цереброинтестинальные гормоны (соматостатин, вещество Р, вазоактивный кишечный пептид и др.). Активность нейронов гипоталамуса может модулироваться деятельностью других нейронов, реагирующих на различные сигналы, такие как растяжение желудка, высвобождение гормонов ЖКТ, утилизация глюкозы и т.д.
Нарушение фунтами гипоталамической области у человека приводит к развитию ожирения. Травматические, воспалительные процессы, опухоли и метастазы злокачественных опухолей могут быть причиной диэнцефального ожирения.
Важное значение в патогенезе ожирения имеют гиперинсулинизм и инсулинорезистентность, связанная со снижением числа инсулиновых рецепторов в жировых, почечных, печёночных клетках и нейронах вентромедиального гипоталамуса. Инсулинорезистентность объясняется препятствующим усвоению глюкозы повышением концентрации НЭЖК в крови тучных людей.
Таким образом, некоторые важные особенности метаболизма при ожирении можно представить в следующем порядке:
1) усиление липогенеза и увеличение размеров адипоцитов при переедании;
2) повышение метаболической активности жировых клеток;
3) увеличение концентрации НЭЖК в крови;
4) потребление мускулатурой главным образом НЭЖК в условиях конкуренции НЭЖК и глюкозы (цикл Рэндла);
5) повышение уровня глюкозы в крови;
6) усиление секреции инсулина и увеличение его концентрации в крови;
7) повышение аппетита. Последнее приводит к перееданию и замыканию "порочного" круга.
Некоторые патогенетические связи и метаболические последствия ожирения представлены в схеме 1.
Схема I. Некоторые патогенетические связи и метаболические последствия ожирения.
«+» -увеличение; «–» – уменьшение; «↓» – способствует.
  Коституциональная предрасположенность, тип высшей нервной деятельности, подвижность, особенности обмена. Коституциональная предрасположенность, тип высшей нервной деятельности, подвижность, особенности обмена. |
 Пищевые привычки, воздействие психических и социальных факторов. Пищевые привычки, воздействие психических и социальных факторов. |
 Органические повреждения головного мозга, гипоталамические нарушения аппетита. Органические повреждения головного мозга, гипоталамические нарушения аппетита. |
    Переедание абсолютное (гиперфагия), относительное (углеводное) Переедание абсолютное (гиперфагия), относительное (углеводное) |
   Инсулино-резистентность Инсулино-резистентность |
| Снижение специфического динамического действия пищи |
   Гормоны: норадреналин, глюкагон, СТГ, кортизол Гормоны: норадреналин, глюкагон, СТГ, кортизол |
| Печень |
| Жировая ткань |
| Мускулатура |
     Гиперинсулинемия Гиперинсулинемия |
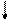 + Использование глюкогенных аминокислот из крови + Использование глюкогенных аминокислот из крови |
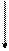 + Синтез триглицеридов и кетогенез + Синтез триглицеридов и кетогенез |
| + Глюконеогенез |
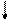 – Торможение липолиза – Торможение липолиза |
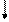 + Липолиз и освобождение шлицерина и жирных кислот + Липолиз и освобождение шлицерина и жирных кислот |
| + Переэстерифи-кация жирных кислот |
 + Липогенез + Липогенез |
| + Торможение освобождения аминокислот |
 + Использование глюкозы + Использование глюкозы |
 + Сгорание жирных кислот и кетоновых тел + Сгорание жирных кислот и кетоновых тел |
| Плазма: Повышение концентрации глюкозы, аминокислот, НЭЖК, глицерина, триглицеридов, холестерина, мочевой кислоты; снижение толерантности к глюкозе, концентрации СТГ. |
 |
При ожирении выявляются нарушения функций гипофиза и периферических эндокринных желез. У больных ожирением часто отмечаются изменения функций половых желез, которые у женщин проявляются нарушением менструального цикла и гирсутизмом (следствие измененной функции гипоталамо-гипофизарной системы). У страдающих ожирением, повышен уровень свободных андрогенов в сыворотке крови вследствие снижения концентрации глобулина, связывающего половые гормоны.
При ожирении развивается резистентность к тироидным гормонам и снижается количество рецепторов в Т3 и Т4. Также снижается исходный уровень и уменьшается секреция СТГ. Возможно, гиперинсулинизм, наблюдающийся при ожирении, способствует повышению концентрации соматомединов, а последние по механизму обратной связи ингибируют секрецию гормона роста. Нарушается секреция пролактина, что является результатом нарушения гипоталамического контроля секреции в высвобождения гормона из гипофиза.
У 70-80% больных, страдающих ожирением, отмечается нарушение толерантности к углеводам, а у 1/4-1/5 выявляется сахарный диабет. Изучение содержания иимунореактивного инсулина в сыворотке крови больных показало двух-трех кратное превышение его концентрации по сравнению с лицами, имеющими нормальную массу тела.
В крови больных с ожирением отмечается повышение уровня холестерина, триглицеридов, мочевой кислоты, липопротеидов очень низкой плотности и снижение количества липопротеидов высокой плотности.
Таким образом, ожирение сопровождается нарушением всех видов обмена веществ и изменением функций большинства эндокринных желез. Глубокие дисгормональные изменения и нарушения метаболизма замыкаются в порочный круг, усугубляющий картину заболевания. Усиливаются эффекты липогенных гормонов - инсулина, глюкокортикостероидов и повышается чувствительность к ним. Снижается действие жиромобилизущих гормонов - половых, адреналина. Гиперсекреция альдостерона способствует задержке воды и натрия, увеличивая массу тела и уменьшая использование жиров на эндогенный синтез воды. Метаболическая иммунодепрессия, наблюдающаяся при ожирении, снижает устойчивость организма к инфекционным агентам и повышает вероятность развития опухолей. Ожирение отражается на функциональном состоянии всех органов и систем, нарушает взаимоотношения регуляторных механизмов и интермедиарный обмен.
Основными принципами лечения ожирения являются субкалорийная диета с пониженным содержанием жиров и углеводов, но полноценная в отношении содержания белков и витаминов, психотерапия, лечебная гимнастика, массаж. Медикаментозное лечение проводится в случае неэффективности диетотерапии. С этой целью применяют тироидные гормоны, повышающие основной обмен и усиливающие специфически-динамическое действие пищи. Показаны препараты, угнетающие аппетит (фепранон, дезопимон и др.).
В последние годы широко применяется адипозин– препарат из гипофиза крупного рогатого скота, стимулирующий липолиз.
Так как похудеть тяжелее, чем предотвратить прибавление масон тела, нужно обратить серьезное внимание на пропаганду здорового образа жизни и проведение профилактических мероприятий.
 2015-07-04
2015-07-04 2981
2981
