После опытов Резерфорда, теории Бора атома водорода и, наконец, создания квантовой теории атома водорода Шредингером и Гайзенбергом возникла ясная качественная картина устройства атомов. Атом состоит из ядра и движущихся около него электронов. Экспериментальные методы исследования атомных спектров давали богатый материал для изучения электронного строения атома. Темным пятном было устройство ядра.
Первая модель ядра основывалась на знании только двух элементарных частиц - электрона и протона (до 1932 г.). Протоны впервые были получены Резерфордом в реакции
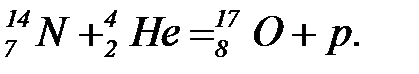 (1)
(1)
Эта реакция состояла в том, что a -частица (ядро атома гелия) налетала на ядро атома азота. В результате чего рождался изотоп кислорода 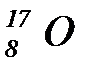 и еще одна частица. Наблюдение треков в камере Вильсона, помещенной в магнитное поле, позволило отождествить эту частицу с ядром атома водорода - простейшим из всех ядер.
и еще одна частица. Наблюдение треков в камере Вильсона, помещенной в магнитное поле, позволило отождествить эту частицу с ядром атома водорода - простейшим из всех ядер.
В соответствии с этими знаниями предполагалось, что ядра атомов состоят из протонов и электронов. Согласно этой модели атом азота, например, состоял из 7 электронов в электронной оболочке, 14 протонов в ядре и 7 ядерных электронов. Такое представление подкреплялось открытием b -распада ряда ядер. В результате b -распада из ядра вылетал электрон. Но модель стала неприемлемой после открытия существования двух типов тождественных частиц - фермионов и бозонов - и открытия их свойств. По электронно-протонной модели выходило, что атом азота должен быть бозоном, а опытные данные говорили, что он является фермионом. Также не удавалось объяснить значения магнитных моментов атомов и ядер. Кроме того, появилось много опытных данных об излучении ядрами рентгеновских фотонов. Оказалось, что аналогично спектрам излучения атомов, спектры излучения ядер являются линейчатыми, то есть составляющие ядра частицы находятся в состояниях с определенными значениями энергии. Но вот изучение энергетических спектров электронов, возникающих в результате b -распада, показало, что эти спектры непрерывны, и объяснить происхождение этих электронных спектров не удавалось. Ядерный электрон, как и другие частицы ядра, должен был находиться на энергетическом уровне. Вылетающие в результате b -распада электроны также должны были бы иметь определенную энергию, чего не происходило.
 2015-07-14
2015-07-14 1134
1134








