В химический стакан помещают 25 или 50 мл анализируемой питьевой воды, подкисляют 2-3 мл азотной кислоты и титруют стандартным раствором AgNO3.После введения каждой порции титранта раствор перемешивают, часть оттитрованного раствора помещают в кювету и измеряют оптическую плотность (контроль – дистиллированная вода).
Раствор из кюветы присоединяют ко всей пробе анализируемой воды, добавляют очередную порцию титранта и т.д. По полученным данным строят кривую титрования – график зависимости оптической плотности от объема введенного титранта—и фиксируют положение точки стехиометричности.
Содержание хлоридов в питьевой воде (Q, мг Cl-/л) вычисляют по формуле:
 Q=
Q= 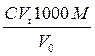 (16)
(16)
Где С—молярная концентрация стандартного раствора AgNO3.
Vt—израсходованный на титрование объем стандартного раствора AgNO3,
V0—взятый для титрования объем питьевой воды,мл;
М—молярная масса хлора, г/моль.
Контрольные вопросы и задания.
1.Перечислить анионы, которые могут содержаться в питьевой воде, и указать методы их определения.
2. Как проводят фототурбидиметрическое титрование хлоридов и какие требования предъявляют при этом?
3. Обосновать характер кривой фототурбидиметрического титрования при определении хлоридов.
 2015-07-14
2015-07-14 906
906








