1. Определить объем водорода, вытесненного взятой навеской металла при температуре «t» и давлении «Р»:
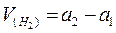 ,
,
где a1 и a2 – соответственно начальный и конечный уровни воды в бюретке, мл.
2. Приведите найденный объем водорода к нормальным условиям по формуле
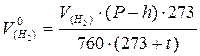 ,
,
где 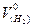 – объем водорода при н.у., мл;
– объем водорода при н.у., мл;
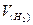 – объем водорода, полученный в опыте, мл;
– объем водорода, полученный в опыте, мл;
P – атмосферное давление по барометру, мм.рт.ст.;
t – комнатная температура, ºС;
h – давление водяных паров при температуре опыта (по таблице), мм рт. ст.
Таблица
Давление водяного пара, мм рт. ст.
| Температура по Цельсию | Давление | Температура по Цельсию | Давление | Температура по Цельсию | Давление |
| 4,6 | 9,8 | 18,65 | |||
| 4,9 | 10,52 | 19,83 | |||
| 5,3 | 11,23 | 21,03 | |||
| 5,7 | 11,99 | 22,38 | |||
| 6,1 | 12,79 | 23,76 | |||
| 6,5 | 13,63 | 25,15 | |||
| 7,0 | 14,53 | 26,58 | |||
| 7,5 | 15,48 | 28,03 | |||
| 8,0 | 16,48 | 29,51 | |||
| 8,6 | 17,54 | 31,04 | |||
| 9,2 |
3. Рассчитайте эквивалентную массу взятого металла по формуле: 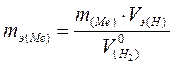 ,
,
Vэ(H) = 11,2 л/моль = 11200 мл/моль.
4. Зная величину удельной теплоемкости исследуемого металла (для металла «а» удельная теплоемкость равна 0,42 Дж/г∙К, для металла «в» – 1,09 Дж/г∙К, для металла «с» – 0,98 Дж/г∙К), определите приближенную массу металла с помощью правила Дюлонга и Пти.
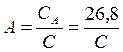 .
.
5. Зная приближенную атомную массу металла и его эквивалентную массу, найдите валентность металла, округлив её значение до целого числа.
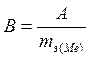 .
.
6. Рассчитайте точную атомную массу металла.
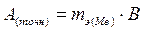 .
.
7. По таблице Д.И. Менделеева определите (в группе, соответствующей полученной валентности), какой металл вы использовали в данной работе. Напишите уравнение реакции взаимодействия найденного металла с кислотой. Найдите погрешность эксперимента.
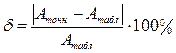 .
.
Полученные результаты занесите в таблицу:
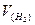
| 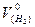
| 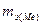
| 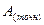
| δ | Уравнение реакции |
 2015-07-14
2015-07-14 435
435








