Строение металлических сплавов зависит от того, в какие взаимодействия вступают компоненты, составляющие сплав (систему).
Компоненты, взаимодействуя друг с другом, могут образовывать твердые растворы, химические соединения и гетерогенные (неоднородные) структуры, состоящие из нескольких фаз.
Твердые растворы образуются в том случае, когда компоненты сплава растворимы друг в друге в твердом состоянии. Рентгеновский анализ обнаруживает в твердом растворе, как и у чистого металла, только один тип кристаллической решетки, металлографический - выявляет структуру из однородных зерен. Если кристаллизуется твердый раствор на базе одного из компонентов, последний является растворителем, а атомы другого (растворенного) компонента располагаются в кристаллической решетке растворителя.
Твердые растворы обозначаются буквами греческого алфавита: a, b, d, g и т.д.; или А(В), где А - растворитель, В - растворенный компонент. Твердые растворы существуют не при строго определенном соотношении атомов компонентов, а в интервале концентраций.
Различают твердые растворы замещения, внедрения и вычитания.
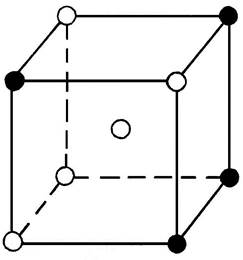
В твердых растворах замещения атомы растворенного компонента занимают положения атомов растворителя в кристаллической решетке (рис.1, а). Твердые растворы замещения характерны для сплавов большинства металлов (Fe, Cr, Мn, Ni, Mo, Cu, Zn, Sn, Al и др.) и могут быть с ограниченной (неполной) или с неограниченной (полной) растворимостью компонентов друг в друге.
 | 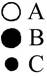 |  | |
| а) | б) |
Рис.1. Кристаллическая решетка твердого раствора замещения (а) и твердого раствора внедрения (б)
Неограниченная растворимость возможна, если оба компонента имеют идентичные, изоморфные кристаллические решетки, малое различие атомных размеров компонентов в пределах 7-17%, близкое расположение компонентов в периодической системе элементов Д.И. Менделеева.
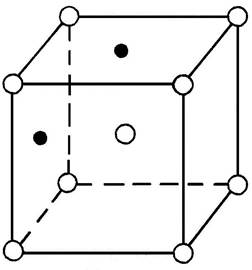
Твердые растворы внедрения получаются в тех случаях, когда диаметр растворенного элемента невелик, и наблюдаются при растворении в железе, молибдене, хроме таких неметаллов, как углерод, азот, водород, т.е. элементов с малым атомным радиусом. Твердые растворы внедрения бывают только с ограниченной (неполной) растворимостью компонентов (рис.1, б).
В сплавах могут также образоваться твердые растворы на базе химического соединения, где химическое соединение является растворителем, сохраняется его кристаллическая решетка, а атомы растворенного элемента располагаются в этой кристаллической решетке.
Твердыми растворами вычитания называются твердые растворы на базе химических соединений, образование которых сопровождается появлением вакансий. Например, таким является твердый раствор на базе химического соединения СoАl.
При образовании твердых растворов замещения и внедрения атомы растворенного элемента располагаются в кристаллической решетке растворителя неупорядоченно, в связи с этим их называют неупорядоченными твердыми растворами.
В некоторых случаях, когда атомы элементов, составляющие сплав, притягиваются друг к другу сильнее, чем подобные атомы, они стремятся расположиться в кристаллической решетке растворителя в определенном порядке. Такие твердые растворы называют упорядоченными или сверхструктурами (рис.2). Полностью упорядоченные растворы образуются, когда соотношение компонентов равно целому числу 1:1, 1:2, 1:3 и т.д. Упорядоченные твердые растворы можно рассматривать, как промежуточные фазы между твердыми растворами и химическими соединениями.
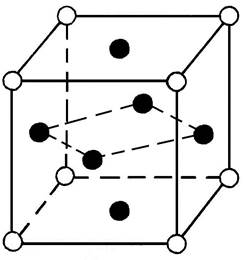 | 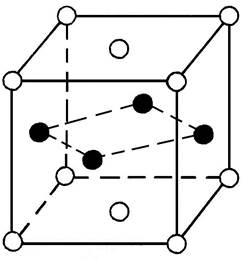 |
| Cu3Au | CuAu |
Рис.5.2. Кристаллические решетки упорядоченных твердых растворов в системе Cu-Al (Cu - l; Al -¡)
Химические соединения образуются в том случае, когда атомы различных элементов притягиваются и имеют электрохимическое различие. Характерным для химических соединений является стехиометрическое соотношение атомов элементов, что выражается простой формулой в общем виде АnВm, где А и В - элементы, n и m - простые целые числа. В химических соединениях кристаллическая решетка, как правило, отличная от кристаллических решеток элементов, атомы в решетке располагаются упорядочение, закономерно в определенных узлах.
Химические соединения имеют постоянную температуру плавления (диссоциации), свойства соединения резко отличаются от свойств образующих его компонентов.
Химическое соединение между металлами имеет в узлах решетки положительно заряженные ионы, удерживаемые электронным газом - металлическая связь. Такие соединения называются интерметаллидами (CuAl2, Mg2Sn и т.д.). Химические соединения металла c неметаллом имеют ионную связь, атомы удерживаются в кристаллической решетке электростатическим притяжением. В соединениях такого типа связь жесткая.
Электронные соединения, т.е. соединения между двумя металлами в сплавах, отличается постоянным соотношением валентных электронов к числу атомов 3/2; 21/13; 7/4. Каждому соотношению соответствует определенная кристаллическая решетка: 3/2 - b-фаза (решетка объемноцентрированного куба), 21/13 - g-фаза (решетка сложная кубическая), 7/4 - d-фаза (гексагональная решетка).
Электронные соединения (фазы Юм-Розери) имеют определенное соотношение атомов и новую кристаллическую решетку - это признаки химического соединения, однако полного упорядочения расположения атомов не наблюдается, поэтому их относят к промежуточным фазам между химическим соединением и твердым раствором.
Фазы Лавеса имеет формулу АВ2 (А и В компоненты) и наблюдаются между элементами, атомные диаметры которых DA/DB=1,2. Эти фазы при кристаллизации образуют кристаллические решетки: гексагональную (MgZn2 и МgNi2) или гранецентрированную кубическую (MgCu2). Фазы Лавеса встречаются в сплавах, как упрочняющие фазы.
Гетерогенные (неоднородные) структуры образуются в том случае, когда компоненты не обладают полной взаимной растворимостью друг в друге в твердом стоянии, например: Zn-Sn; Pb-Sn; Fe-C; Al-Cu и др. Число кристаллических решеток соответствует числу фаз, образующихся в гетерогенной структуре.
Если компоненты незначительно растворяются друг в друге в твердом состоянии (Ge-Zn), то фактически получается микросмесь, состоящая из двух чистых компонентов.
При количестве компонентов, превышающих их предельную растворимость, наблюдается структура из двух насыщенных твердых растворов или твердого раствора и химического соединения и т.д. Такая структура может быть эвтектического или перитектического типа.
 2015-07-14
2015-07-14 1636
1636








