· Первый постулат Бора. Электрон в атоме водорода движется, не излучая, по круговой орбите, для которой момент импульса электрона
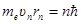 , или
, или 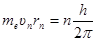 ,
,
где me – масса электрона;
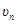 – скорость электрона на n -ой орбите;
– скорость электрона на n -ой орбите;
rn – радиус n -ой стационарной орбиты;
ħ = 1,05×10-34 Дж×с, или h = 6,63×10-34 Дж×с – постоянная Планка;
n = 1, 2, 3,… – квантовое число (номер орбиты электрона).
· Второй постулат Бора. При переходе электрона с одной орбиты на другую атом водорода излучает или поглощает квант энергии:
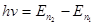 ,
,
где 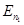 и
и 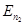 – полные энергии электрона в атоме на соответствующей орбите.
– полные энергии электрона в атоме на соответствующей орбите.
· Полная энергия электрона в атоме водорода
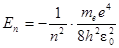 (n = 1, 2, 3,…),
(n = 1, 2, 3,…),
где n – номер орбиты;
me – масса электрона;
е – заряд электрона;
ε0 = 8,85×10-12 Ф/м – электрическая постоянная;
h – постоянная Планка.
· Формула, позволяющая найти частоты v или длины волн λ, соответствующие линиям водородного спектра (сериальная формула Бальмера)
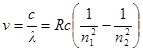 ,
,
где R – постоянная Ридберга (R = 1,10×107 м-1);
с – скорость света в вакууме;
n1 и n2 – квантовые числа, определяющие номера орбит электрона.
Для водородоподобных ионов формула имеет вид:
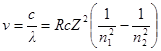 ,
,
где Z – порядковый номер в таблице Менделеева.
· Длина волны де Бройля
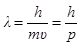 ,
,
где p=m 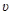 – модуль импульса движущейся частицы.
– модуль импульса движущейся частицы.
· Импульс частицы и его связь с кинетической энергией T:
а) 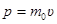 ;
; 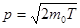 ;
;
б) 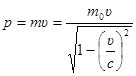 ;
; 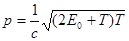 ,
,
где m 0 – масса покоя частицы;
m – релятивистская масса частицы;
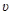 – скорость частицы;
– скорость частицы;
с – скорость света в вакууме;
Е 0 – энергия покоя частицы (Е 0 = m 0 с2).
· Соотношение неопределенностей:
а) для координаты и импульса
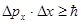 ,
,
где D Рх – неопределенность проекции импульса на ось Х;
D х – неопределенность координаты;
б) для энергии и времени
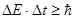 ,
,
где D Е – неопределенность энергии;
D t – неопределенность времени жизни квантовой системы в данном энергетическом состоянии.
· Одномерное уравнение Шредингера для стационарных состояний
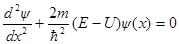 ,
,
где ψ(х) – волновая функция, описывающая состояние частицы;
m – масса частицы;
Е – полная энергия частицы;
U = U(х) – потенциальная энергия частицы.
· Плотность вероятности
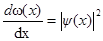 ,
,
где d ω(x) – вероятность того, что частица может быть обнаружена вблизи точки с координатой x на участке dx.
· Вероятность обнаружения частицы в интервале от х 1 до х 2
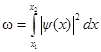
· Решение уравнение Шредингера для одномерного бесконечно глубокого, прямоугольного потенциального ящика:
а) 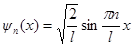 – собственная нормированная волновая функция;
– собственная нормированная волновая функция;
б) 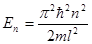 – собственное значение энергии, где n – квантовое число (n = 1, 2, 3,…); l – ширина ящика.
– собственное значение энергии, где n – квантовое число (n = 1, 2, 3,…); l – ширина ящика.
В области 0 £ x £ l U = ∞ и ψ (х) = 0.
· Коэффициент прозрачности прямоугольного потенциального барьера, т.е. вероятность прохождения (туннелирования) микрочастицы сквозь барьер:
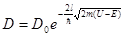 ,
,
где D 0 – коэффициент, по порядку величины близкий к единице;
U – высота потенциального барьера;
l – его ширина;
Е – энергия частицы;
m – масса частицы.
· Закон радиоактивного распада
dN = – λ × N × dt, или 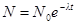 ,
,
где dN – число ядер, распадающихся за интервал времени dt;
N – число ядер, не распавшихся к моменту времени t;
N 0 – число ядер в начальный момент (t = 0);
λ – постоянная радиоактивного распада.
· Число ядер, распавшихся за время t:
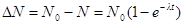 .
.
· Период полураспада
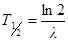 .
.
· Среднее время жизни радиоактивного ядра, т.е. интервал времени, за который число нераспавшихся ядер уменьшилось в е раз:
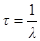 .
.
· Число атомов, содержащихся в радиоактивном изотопе
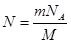 ,
,
где m – масса изотопа;
М – молярная масса;
NA – постоянная Авогадро (NA =6,02×1023 моль-1).
· Активность радиоактивного изотопа
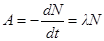 , или
, или 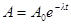 ,
,
где dN – число ядер, распадающихся за интервал времени dt;
А 0 – активность изотопа в начальный момент времени (t = 0), А 0 =λN 0.
· Удельная активность изотопа
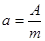 .
.
· Дефект массы ядра
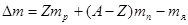 ,
,
где Z – зарядовое число (число протонов в ядре);
А – массовое число (число нуклонов в ядре);
(А-Ζ) – число нейтронов в ядре;
mр – масса протона;
mn – масса нейтрона;
mя – масса ядра.
· Энергия связи ядра
Есв = D mс2,
где Δ m – дефект массы ядра;
с – скорость света в вакууме.
Во внесистемных единицах энергия связи ядра равна Есв = 931×Δ m Мэв, где дефект массы Δ m – в а.е.м.; 931 – коэффициент пропорциональности (1 а.е.м. ~ 931 МэВ).
· Правило смещения:
1) для α -распада: 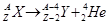 ;
;
2) для β- -распада: 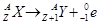 ;
;
3) для β+ -распада: 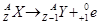 .
.
· Ядерные реакции. Символическая запись ядерной реакции может быть дана или в развернутом виде, например:
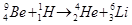
или сокращенно
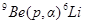 .
.
При сокращенной записи порядковый номер атома не пишут, так как он определяется химическим символом атома. В скобках на первом месте ставят обозначение бомбардирующей частицы, на втором – обозначение частицы, вылетающей из составного ядра, и за скобками – химический символ ядра-продукта.
Обозначения частиц: р – протон, n – нейрон, d – дейтрон, t – тритий (тритон), α -альфа-частица, γ-гамма-фотон.
· Энергетический эффект ядерной реакции
Q = c 2[(m 1 +m 2) –(m 3 +m 4)],
где m 1 – масса покоя ядра-мишени;
m 2 – масса покоя бомбардирующей частицы,
(m 3 + m 4) – сумма масс покоя ядер продуктов реакции.
Если m 1 + m 2 > m 3 + m 4, то энергия освобождается, реакция экзотермическая. Если m 1 + m 2 < m 3 + m 4, то энергия поглощается, реакция эндотермическая.
· При решении задач на ядерные реакции применяются законы сохранения:
1) электрического заряда: z 1 + z 2 = z 3 + z 4;
2) суммарного числа нуклонов: А 1 + А 2 = А 3 + А 4;
3) релятивистской полной энергии: Е 1 + Е 2 = Е 3 + Е 4; или
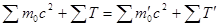 ,
,
где 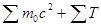 – сумма энергий покоя частиц и их кинетических энергий до реакции; справа то же для частиц после реакции;
– сумма энергий покоя частиц и их кинетических энергий до реакции; справа то же для частиц после реакции;
4) импульса: р 1 + р 2 = р 3 + р 4.
 2015-07-14
2015-07-14 684
684








