Одной из первых физически обоснованных моделей атома явилась модель атома Дж. Дж. Томсона, разработанная им после открытия электрона. Томсон представлял атом в виде положительно заряженной сферы, внутри которой располагались электроны, число которых было таким, что общий электрический заряд атома был равен нулю. Радиус сферы составлял порядка 10 10м. В простейшем атоме водорода электрон, несущий отрицательный заряд, по представлению Томсона, должен находиться в центре сферы.
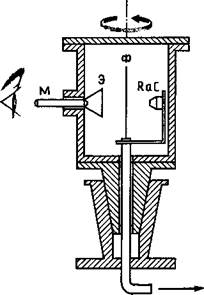
В 1911 г. Резерфорд с сотрудниками в Кавендишской лаборатории осуществил эксперименты по прохождению а-частиц через тонкую золотую фольгу. Упрощенная схема эксперимента показана на рисунке 117. Частицы, испускаемые радиоактивным препаратом, содержащим радий, проходили через золотую фольгу Ф и попадали на экран v9, покрытый сернистым цинком — веществом, способным испускать кванты света при соударении с а-частицами. В этом случае в местах попадания а-частиц на экран наблюдаются слабые, но вполне доступные наблюдению вспышки света. Наблюдения проводились с помощью микроскопа М. Подсчитывая число вспышек света за определенный промежуток времени в зависимости от угла рассеяния 0, можно было установить характер распределения положительного заряда внутри атома.
 К насосу К насосу
|
| Схема опыта Резерфорда по рассеянию а-частиц |
В результате экспериментов выяснилось, что положительный заряд атома, играющий роль рассеивающего центра, не размещен внутри сферы радиусом ~10~10м, а сосредоточен в объеме гораздо меньшего радиуса, порядка. Атом водорода по 10 ^— 10~15 м. Было высказано предположение, что атом имеет положительно заряженное ядро, в котором сосредоточена практически вся масса атома. Это приводило к тому, что а-частицы, налетающие на ядро, иногда отскакивали от него, как мячики от стенки, испытывая отклонение на 180° от первоначального направления движения. Результаты проведенных опытов привели Резерфорда к новым представлениям о строении атома, к разработке так называемой планетарной модели атома. Название этой модели связано со строением атома, аналогичным структуре Солнечной системы. Электроны, подобно планетам, движутся в атоме вокруг ядра по своим орбитам. Однако такие представления приводят к противоречию между классической электродинамикой и наблюдаемым поведением атомов вещества. Действительно, двигаясь по орбите вокруг ядра, электрон имеет некоторое ускорение. При движении по круговой орбите это ускорение будет центростремительным. Но при ускоренном движении электрон должен испускать электромагнитные волны. Излучение электромагнитных волн приведет к уменьшению кинетической энергии движения электрона, к уменьшению частоты излучения и в конечном счете к падению электрона на ядро. По расчетам, проделанным на основании законов классической электродинамики, выходило, что электрон должен упасть на ядро за время порядка 10~9 с, т. е. атомы должны быть весьма нестабильными образованиями. За время своего существования атомы должны испускать излучение, имеющее непрерывный спектр.
Опыт же показывает, что это совсем не так. В действительности атомы являются стабильными структурами, а их спектры излучения представляют совокупность отдельных спектральных линий.
В 1885 г. швейцарский физик Иоганн Бальмер (1825— 1898) установил закономерность, позволяющую определять частоты наблюдаемых линий излучения в спектре атомов водорода. Бальмер нашел, что частоты линий подчиняются закономерности
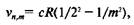
где с — скорость света; т — целые числа, принимающие значения, большие двух: 3, 4, 5,... и т. д., для соответствующих линий оптического спектра водорода; R — постоянная Ридберга, названная в честь шведского физика И. Р. Ридберга (1854—1919) и равная 10973731,77 м-'.
Стабильность атомов и их спектральные закономерности находились в явном противоречии с планетарной моделью атома и классическими представлениями. Выход из создавшегося положения был найден на пути отказа от классических методов описания поведения электрона в атоме.
 2015-07-21
2015-07-21 558
558








